Stofflehre¶
Material, Chemikalien und Hinweise¶
A. Silikate¶
Material
A.1 Demo¶
- Töpfer-Ton
- Quarz-Kristall
- Feldspat-Kristall (falls vorhanden)
- Zeolith falls vorhanden
A.2 bis A.4 Silicagel - Fällungen - chemischer Garten¶
Pro Gruppe
- Becherglas 200 mL
- Becherglas 100 mL
- Glasstab
Pro Klasse
- Käufliches Wasserglas (27 Massen% SiO2)
- Becherglas 1L
- In zwei Abzügen je HCl (conz) (Salzsäure konzentriert) mit Pipette in kleinem Erlenmeyer
-
Klumpen / Kristalle je mit Polylöffel auf Papierserviette von
- Kupfer(II)-sulfat
- Nickel(II)-sulfat
- Eisen(III)-chlorid
- Calciumnitrat
-
Tropffläschchen mit 0.1 M Lösungen von
- Kupfer(II)-Salz
- Nickel(II)-Salz
- Cobalt(II)-Salz
- Eisen(III)-Salz
- Calcium-Salz
- Magnesium-Salz
- Aluminium-Salz
- Ammonium-Salz
- Kalium-Salz
- Tropffläschchen NaCl gesättigt
A.5 elementares Silicum aus Quarz gewinnen¶
Pro Gruppe
- schwerschmelzbares RG
- Stativmaterial
- feuerfeste Unterlage im Abzug
- langer Glasstab
- Abdampfschale (Ø 8 cm)
- Messzylinder 20 ml
- Reagenzglasklammer
- Nutsche auf Saugflasche in Stativ an Wasserstrahlpumpe
- Filterpapier zu Nutschen
- Spatel
Pro Klasse:
- Feines Quarzpulver (Fluka 83340) oder gut getrocknetes Kieselgel mit Mörser
- Magnesiumpulver
- konz. Salzsäure (32%)
A.6 Glasherstellung¶
Pro Klasse:
- Muffelofen, vorgeheizt auf 900°C
- Daneben eine feuerfeste Unterlage und ein Eisenblech, um die Glasperlen auszugiessen
- Gartenhandschuhe (2 Paare)
- 2 Tiegelzangen
- Dazu zwei Polylöffel, um das Glas aus dem Tiegel zu kratzen.
Je bei einer Waage mit Polylöffel auf Papierserviette und 6 kleinen Bechergläsern zum Einwägen.
- Borsäure
- Quarzsand
- Calciumcarbonat
- Natriumcarbonat
- Lithiumcarbonat
- Kupfer(II)-oxid (nur mit Polylöffel, ohne Becherglas) (nicht!!! Kupfer(I)-oxid)
- Eisen(III)-oxid
Pro Gruppe
- 1 Tiegel, möglichst solche, die von früheren Versuchen bereits Glasmasse enthalten, da die Tiegel nur schwer zu reinigen sind bzw. durch das Reinigen kaputt gehen können.
Mischung für 6-8 Ansätze (Original): Wäge folgende Stoffe je in einem Becherglas ein:
- 40 g Borsäure
- 4 g Quarzmehl
- 7 g Calciumcarbonat
- 7 g Natriumcarbonat
- 6 g Lithiumcarbonat
- Optional: eine Spatelspitze Kupfer(II)-oxid (für eine blaue Farbe), Eisen(III)-oxid (gelbe Farbe) oder Mangan(IV)-oxid (Schwarz-braun).
- Mische die Stoffe gut durch Umschütten von einem Becherglas ins andere.
Durchführung und Hinweise
A.1 Demo¶
Etwas Töpfer-Ton wird a) in deionisiertes Wasser und b) in gesättigte Kochsalzlösung gelegt. Erkläre das unterschiedliche Verhalten (nach ca. 30 Minuten). Tipp: der Befund lässt sich mit Osmose erklären.
Mit deionisiertem Wasser entsteht eines stabile Suspension des Tones in Waser (der Ton verteilt sich im Wasser), bei der Salzlösung bleibt der Tonklumpen kompakt und wird nicht von selber suspendiert. Die hohe Ionenkonzentration zwischen den Tonschichten bewirkt wie bei der Osmose, dass sich die Schichten mit Wasser vollsaugen, bis sie sich voneinander lösen und in Suspension gehen, ausser, die Lösung enthält viele Ionen. Es handelt sich also um einen entropischen Efffekt – er wird aber elektrostatische Abstossung genannt, wie bei der Stabilisierung von Seifenblasen und vielen andere
A.2 Fällung von Kieselsäure mit HCl¶
Vorbereitung:
Käufliches Wasserglas (27 Massen% SiO2) wird mit deionisiertem Wasser auf das doppelte Volumen verdünnt. Diese verdünnte Wasserglas-Lösung wird im folgenden für Versuche verwendet.
Experiment 1: Herstellung eines Silicagel
Ca. 50 mL verdünnte Wasserglas-Lösung werden in ein Becherglas gegeben. Zu dieser Lösung wird im Abzug Salzsäure (konz.) zugetropft (zuerst nur einzelne Tropfen zugeben). Dazwischen kann mit einem Glasstab umgerührt werden.
A.3 Fällungsreaktionen mit Kationen¶
Experiment 2: Fällung von Silikaten Es stehen verschiedene Salzlösungen auf.
- Wähle mindestens 2 Lösungen aus, die vermutlich mit Wasserglas keinen Niederschlag geben, und mindestens 2 Lösungen, die mit Wasserglas vermutlich einen Niederschlag geben.
- Halte die Lösungen und Vermutungen schriftlich fest.
- Gib die Lösungen dann tropfenweise zu kleinen Mengen an Silikat-Lösung und halte Beobachtungen fest.
- Notiere die Fällungsreaktionen.
A.3 Chemischer Garten¶
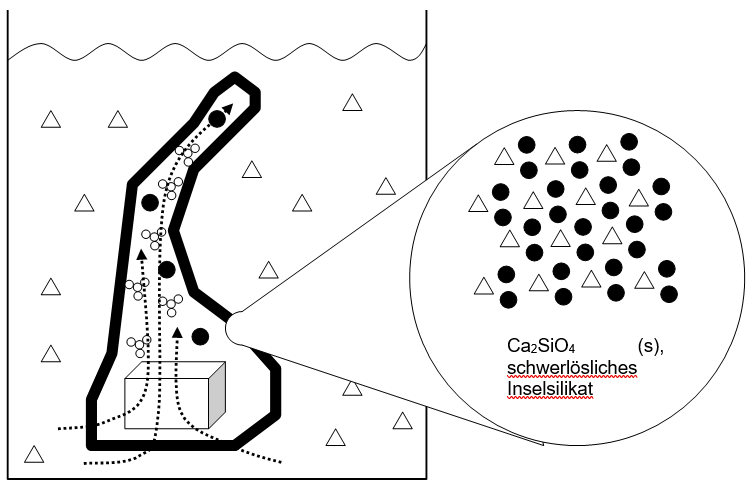
Durchführung: In ein Becherglas werden rund 140 mL verdünnte Wasserglas-Lösung gegeben. Zu dieser Lösung werden Kristalle oder Klumpen von Kupfer(II)-sulfat (blau), Nickel(II)-sulfat (grün), Eisen(III)-chlorid (gelb) oder Calciumnitrat (weiss) gegeben.
Wasser aus der Lösung dringt in die Kristalle ein und beginnt sie zu lösen. Die entstehende Salzlösung ist weniger dicht als das umgebende verdünnte Wasserglas und steigt daher auf. Dort, wo die Salzlösung auf die Wasserglas-Lösung trifft, bilden sich schwerlösliche Salze aus Metall-Kationen und Silikat-Ionen (also schwerlösliche Inselsilikate: Ca2SiO4, Fe4(SiO4)3, Ni2SiO4, Cu2SiO4). Diese Inselsilikate sind nicht wasserdicht, so dass weiterhin Wasser zu den Kristallen diffundiert und diese auflöst. So entsteht innerhalb der Schläuche ein Überdruck, bis die Schläuche schliesslich an irgend einer Stelle zerbersten, frische Lösung ausströmt, dort mit dem Wasserglas zusammentrifft und an der Grenze wieder eine harte Inselsilikat-Schicht ausbildet.
A.5 elementares Silicum aus Quarz gewinnen¶
Arbeitsvorschrift
- In eine Reibeschale werden 2.0 g feines Siliciumdioxid (Quarzsand oder Kieselgel) und 1.8 g Magnesiumpulver eingewogen. Die beiden Edukte müssen durch Umschütten gemischt werden, bis ein homogenes Gemenge entstanden ist. Die Mischung wird dann in einem Abzug mit feuerfester Unterlag in ein schwer schmelzbares RG gegeben oder auf einer feuerfesten Unterlage aufgehäuft.
- Das Gemisch wird im Abzug mit einer rauschenden Flamme erhitzt (falls ein RG verwendet wird, so wird dieses Abzug mit einer kleinen Klammer senkrecht an einem Stativ eingespannt. Das Stativ muss auf einer feuerfesten Unterlage stehen. Der Brenner und das RG sind genau auszurichten) Vorsicht! Der Schlauch des Gasbrenners darf nicht in der Nähe des Gemisches liegen!!! Das Gemisch beginnt plötzlich und schlagartig zu reagieren. Es kann eine Stichflamme aus dem Reagenzglas schiessen, und ausserdem kann es zu einem starken Funkenregen kommen. Daher muss sich die Schutzscheibe des Abzugs ganz unten befinden!
- Sobald die Reaktion in Gang gekommen ist wird der Gasbrenner ausser Betrieb genommen. Nun lässt man das Reagenzglas abkühlen, bis es von Hand angefasst werden kann.
- Nun wird wird möglichst viel vom Produktgemisch aus dem Reagenzglas in eine Abdampfschale oder ein Becherglas geschabt. Eventuell muss das Reagenzglas zertrümmert werden, um an genügend Produkt zu gelangen.
- In einem 25 ml-Messzylinder werden 14 ml Wasser vorgelegt und anschliessend gibt man mit einer Pasteurpipette 6 ml konzentrierte Salzsäure zu. Achtung: konzentrierte Salzsäure wirkt stark ätzend.
- Im Abzug stellt man die Abdampfschale direkt auf die feuerfeste Unterlage. Nun giesst man die verdünnte Salzsäure portionenweise möglichst gleichmässig über das Rohprodukt. Vorsicht! Dabei kommt es zur Bildung hoch reaktiver Nebenprodukte, die sich spontan entzünden. Es ist darauf zu achten, dass sich die Hand nicht direkt über der Abdampfschale befindet. Mit Vorteil wird deshalb zum Ausgiessen der Salzsäure der Messzylinder in eine RG-Klammer eingespannt. Beim ganzen Vorgang soll die Schutzscheibe des Abzugs möglichst weit nach unten gezogen sein.
- Wenn sich das Reaktionsgemisch beruhigt hat, wird mit dem Glasstab vorsichtig umgerührt. Damit können vorhandene, nicht umgesetzte Klümpchen noch zur Reaktion gebracht werden. Um auch wirklich alle Rückstände von MgO zu zersetzen, wird die Mischung mit dem Brenner vorsichtig erhitzt. Sobald die Reaktion endgültig abgeklungen ist, giesst man die abgekühlte Aufschlämmung möglichst vollständig in eine Nutsche und spült mit etwas Wasser nach. Das unlösliche Silicium bleibt auf dem Filterpapier zurück, während die unerwünschten Komponenten des Gemischs in der wässrigen Lösung in die Saugflasche gespült werden.
- Die Nutsche wird ausser Betrieb genommen. Dann wird das gereinigte, aber noch feuchte Silicium in die Abdampfschale geschabt, die vorgängig gereinigt und getrocknet wurde.
- Die Abdampfschale wird nun auf dem Vierfuss mit dem Gasbrenner vorsichtig erhitzt, bis das Silicium trocken ist.
Entsorgung
- Das gewonnene Silicium kann mitgenommen oder in den entsprechend beschrifteten Sammelbehälter gegeben werden.
- Die Mutterlauge des Abnutsch-Vorgangs kann mit Leitungswasser verdünnt und in den Abguss geschüttet werden. Aufgabe
Die durchgeführte Reaktion ist offensichtlich stark exotherm. Das heisst, dass Magnesiumoxid energetisch viel günstiger ist als Siliciumdioxid. Erkläre diesen Umstand mit dem Aufbau der beiden Stoffe.
Silikate wie Quarz sind sehr stabil – viel stabiler als Silicium und Sauerstoff. Daher liegt ja ein so grosser Teil unserer Erde Form von Silikaten vor. Trotzdem ist es aber möglich, aus diesen Verbindungen reines Silicium herzustellen, dass dann in der Halbleiterindustrie zur Herstellung von elektronischen Bauteilen oder Solarzellen verwendet wird.
Bei der Herstellung von Silicium aus Quarzsand müssen die Sauerstoffatome entfernt werden. Die Reaktion zu elementarem Sauerstoff wäre extrem ungünstig und technisch kaum möglich, da die entstehenden Bindungen viel weniger stabil wären als die Bindungen in Quarz. Daher lässt man den Quarz bei der industriellen Reaktion mit Koks (Kohle) reagieren, so dass Sauerstoff in Produkt CO auch wieder eine stark polar Bindung ausbildet. Dennoch gelingt die Reaktioin nur unter grossem Energie-Aufwand:
(1) SiO₂ (s) + 2 C (s) → Si (s) + 2 CO (g) \(ΔH_R\) = 690.4 kJ/mol
Die dazu benötigten Temperaturen von rund 2000°C werden in einem elektrischen Lichtbogenofen erzeugt. Im Labor kann Silicium aber relativ einfach in einer Reaktion zwischen Quarz und elementarem Magnesium gewonnen werden:
(1) SiO₂ (s) + 2 Mg (s) → Si (s) + 2 MgO (s) \(ΔH_R\) = -292,7 kJ/Mol
Die Valenzelektronen sind in Magnesiumatomen noch schwächer gebunden als in Kohlenstoff und werden ganz auf das stark elektronegative O-Atom übertragen. Diese Reaktion ist denn auch exotherm und verläuft nach der notwendigen Aktivierung sehr heftig. Das erhaltene Reaktionsgemisch enthält neben dem gewünschten elementaren Silicium aber auch unerwünschtes Magnesiumoxid MgO, das in reinem Wasser praktisch unlöslich ist, jedoch sehr gut löslich in verdünnter Salzsäure. Dort läuft nämlich die folgende Reaktion ab:
(2) 2 HCl (aq) + MgO (s) → Mg₂⁺ (aq) + 2 Cl⁻ (aq) + H₂O (l)
Das Silicium selbst, ein graubraunes Pulver, wird durch Salzsäure nicht angegriffen und bleibt als Festkörper zurück. Durch die nachfolgende Filtration kann deswegen das Silicium aus dem Gemisch abgetrennt und als Reinstoff isoliert werden. Beim der Zugabe von Salzsäure kommt es aber u.U. auch zu einem Knall mit Feuererscheinung. Denn im Reaktionsansatz kann in einer Nebenreaktion Magnesiumsilicid Mg₂Si – ein blauvioletter Feststoff – gebildet werden:
(3) SiO₂ (s) + 4 Mg (s) → Mg₂Si (s) + 2 MgO (s)
Diese Mg-Si-Verbindung reagiert nun mit Salzsäure zu gasförmigem Silan SiH₄ :
(4) Mg₂Si (s) + 4 HCl (aq) → SiH₄ (g) + 2 MgCl₂ (aq)
Silan SiH4 ist zu Methan CH4 analog, aber im Gegensatz zu diesem sehr instabil und verbrennt an der Luft mit einem Knall spontan zu SiO2 und Wasser:
(5) SiH₄ (g) + 2 O₂ (g) → SiO₂ (s) + 2 H₂O (l)
A.6 Glasherstellung¶
Durchführung: Herstellung von 3-4 Glasperlen
Muffelofen auf ca. 900°C vorheizen
Mischung für 1 Ansatz: Wäge folgende Stoffe je in einem Becherglas ein:
- 7 g Borsäure
- 0.7 g Quarzmehl
- 1.2 g Calciumcarbonat
- 1.2 g Natriumcarbonat
- 1.1 g Lithiumcarbonat
- Optional: eine Spatelspitze Kupfer(II)-oxid (für eine blaue Farbe), Eisen(III)-oxid (gelbe Farbe) oder Mangan(IV)-oxid (Schwarz-braun).
Mische die Stoffe gut durch Umschütten von einem Becherglas ins andere und giesse sie dann in einen Tiegel. Die Mengen sind so bemessen, dass die Masse im Tiegel nicht überkochen kann (keinesfalls mehr nehmen!).
Vorsicht: am Muffelofen nur mit Gartenhandschuhen hantieren!
Vorsicht: Heissen Tiegel keinesfalls auf eine ungeschützte Tischoberfläche stellen! Dieser würde dadurch gesprengt! Die heissen Tiegel müssen auf feuerfesten Unterlagen abgestellt werden.
Vorsicht: nach dem Giessen den heissen Tiegel wieder in den Muffelofen stellen und mit diesem zusammen abkühlen. Andernfalls zerspringt der Tiegel.
Stelle den Tiegel mit der Tiegelzange in den vorgeheizten Muffelofen. Beobachte die Probe immer wieder, öffne den Ofen aber nicht zu oft und nicht zu lange, da sonst jedes Mal viel Hitze verloren geht und der Prozess anhält.
Sobald die Glasmasse homogen aussieht und sich nicht mehr verändert, können die Glasperlen auf das Metallblech gegossen werden. Nochmals: Vorsicht: heissen Tiegel niemals direkt auf den Tisch stellen.
Fragen: 1. Glas wird aus einer ganzen Reihe verschiedener Edukte hergestellt. Gib für jedes dieser Edukte an, ob es sich dabei um einen molekularen Stoff, einen salzartigen Stoff oder ein Metall handelt.
- Welche Reaktionen laufen beim Aufschäumen der Glasmasse ab und welches Gas entsteht bei dieser Reaktion?
B. Schwefel¶
Material
B.1 Modifikationen von Schwefel¶
- Reagenzglas
- Bunsenbrenner mit Feuerzeug
- elementarer Schwefel
Durchführung und Hinweise
B.1 Modifikationen von Schwefel¶
- Das REagenzglas wird 3-4 cm hoch mit Schwefelpulver gefüllt
- Das Becherglas wird mit Wasser gefüllt
- Man erhitzt den Schwefel unter ständigem Schütteln langsam (Schwefel ist ein schlechter Wärmeleiter) und beachtet Farbänderungen und Viskositätsveränderungen
- sobald der Schwefel siedet, wird er in das bereitstehende Wasserbad gelehrt
-
Wenn sich der Schwefel beim Erhitzen entzündet, durch Abdecken löschen
-
bei 114°C schmilzt Schwefel zu einer gelben, leicht beweglichen Flüssigkeit (Cyclische Moleküle), wird dann allmählich braun, immer dunkler und zähflüssiger (Ringe brechen auf und Ketten setzen sich zu langen Ketten zusammen). Bei ca 444°C verdampft der Schwefel (gasförmiges S₂) und setzt sich oben im RG als "Schwefelblüte" oder "Schwefelblume" ab. Im abgeschreckten Schwefel bleiben die langen Ketten noch eine Weile bestehen, daher ist das Material noch für etwa einen Tag gummiartig plastisch. sobald sich die ringe wieder gebildet haben, hat der Schwefel die alten Eigenschaften zurück.
Material
Durchführung und Hinweise



Sicherheit¶
Sicherheitshinweise
Weiteres¶
Infos
- Nanoo-Zugang: nanoo.tv/sso/waad/
- Zugangslink, Video, Metadaten