2. Licht und Farbe¶
Material, Chemikalien und Hinweise¶
A. Weiss ist ein Gemisch bunter Farben¶
Material
A.1 Weisses Licht mit Gitter zerlegen¶
- Hellraumprojektor
- Blende für Gitterversuche (Abdeckende Platte mit einem Schlitz)
- Optisches Gitter und Gitterständer für Hellraumprojektor
- Optische Gitter im Dia-forma für auf den Hellraumprojektor und für die SuS, um selber Spektren heller Lichtquellen aufzutrennen
- Handspektroskope
A.2 Farbige Lichter mischen¶
- 3 LED-Spotlampen (benötigt werden rot, grün, blau zum Farbenmischen und weiss zum Auftrennen)
- Weisse Platte als Bildschirm = Screen (um mit den Spotlampen darauf zu zünden und so Farben zu mischen.)
Durchführung und Hinweise
A.1 Weisses Licht mit Gitter zerlegen¶
Lichtstrahl des Hellraumprojektor durch optisches Gitter in Spektralfarben zerlegen und auf Leinwand projizieren. Dann mit Farbfolien das Spektrum direkt nach Prisma abdecken. Wenn z.B. die rote Folie nur rot durchlässt, so wird die Komplementärfarbe absorbiert (= Mischfarbe, die grünblau ergibt).
A.2 Optisches Prisma¶
- Lichtpunkt (helles LED, )
- Optisches Prisma: lichtpunkt hindurchzünden und direkt oder durch das Gitter anschauen: Prisma unmittelbar vor das Auge halten, das Objekt suchen, Prisma mit oder ohne Gitter langsam vom Auge entfernen und so den Verlauf der Strahlen überlegen. Nur direkte Sonnenstrahlung lässt sich sichtbar projizieren.
A.3 Farbige Lichter mischen¶
Mit roter, grüner, blauer LED-Lampe Farben additiv mischen lassen – für paarweise Mischungen Farben vorhersagen lassen, dann alle drei. Hand in Lichtstrahl halten (die weisse Mischung erscheint dadurch viel deutlicher weiss und es ergeben sich verschiedenfarbige Schatten). Man kann also über violett wieder von der langwelligsten Farbe zurück zur kurzwelligsten: kreisförmige Anordnung!
A.4 Weisses und farbiges Licht mit Spektrometer analysieren¶
- Pasco-Photospektrometer mit Lichtleiter zum Ausmessen des Spektrums von Leuchtquellen (z.B. LED-Spotlampen)
B. Elektromagnetische Strahlung¶
Material
B.1 Andere elektromagnetische Strahlung als sichtbares Licht¶
- Gleiche Ausrüstung wie A.1 Weisses Licht mit Gitter zerlegen
- UV-Taschenlampe
- Säckchen mit optischem Aufheller oder fluoreszierende Fläche
B.2 Elektromagnetische Strahung hat Wellennatur und die wahrgenommene Farbe (und sonstige Eigenschaften) hängen von der Wellenlänge ab¶
- optisches Gitter
- roten und grünen Laserpointer
- Weisses Papier an senkrechtem Screen zum Projizieren und einzeichen
- Roter Stift
- grüner Stift
Durchführung und Hinweise
B.1 Andere elektromagnetische Strahlung als sichtbares Licht¶
- Vor der UV-Taschenlampe leuchtet der Aufheller (oder andere fluoreszente Probe) Hell auf. die Taschenlampe sendet also irgend eine Strahlung, die Energie zum Aufheller transportiert und dort die zum Leuchten nötige Energie liefert. Wo kommt diese Strahlung vor? Ist sie vielleicht auch Bestandteil von weissem Licht aus verschiedenen Quellen?
- im von einem optischen gitter aufgetrennten Hellraumprojektor-Licht knapp neben dem Violetten Licht den Aufheller halten. Im Bereich des UV leuchtet der Aufheller schwach auf: offenbar kommt hier eine andere Strahlung an und liefert die Energie, welche den Aufheller zum Leuchten bringt
B.2 Elektromagnetische Strahung hat Wellennatur und die wahrgenommene Farbe (und sonstige Eigenschaften) hängen von der Wellenlänge ab¶
- Der Strahlengang des (aufgetrennten) Strahls eines roten Pointers durch das Gitter wird untersucht. Was passiert, wenn man die Distanz zwischen Pointer und Prisma erhöht? Zwischen Prisma und Screen?
- Für ein genau definiertes Setting (Gitter fixiert in bestimmtem Abstand vom Screen) werden die roten Punkte auf dem Screen mit roter Farbe eingezeichnet.
- Der Strahlengang des Strahls eines grünen Pointers, der genau am selben Ort durchläuft, wird ebenfalls festgehaltn (grüne punkte mit grüner Farbe einzeichnen)
- wenn man das mit Lasern aller Farben machen würde, wie würde das bild vermutlich aussehen?
- Mit hilfe der Animationen vom Doppelspalt plausibel machen, dass das ein Interferenzbild ist. Anhand von grafischen Erklärung des Interferenzmusters überlegen lassen, welches Licht die grössere Wellenlänge hat: Rot oder grün.
C. Streuung und Reflexion von Licht¶
Material
C.1 Licht wird sichtbar durch Streuung an Ammoniumchlorid¶
- HCl conz (Salzsäure)
- NH3 conz (Ammoniak)
- Laserpointer
C.1 Farben durch Streuung¶
- möglichst grosses Becherglas (möglichst breit)
- Wenig Milch mit Tropfpipette
- Spotlampe LED weiss
- Glasstab zum Umrühren
- Weisses blatt oder weisse Tafel als Bildschirm
Durchführung und Hinweise
C.1 Licht wird sichtbar durch Streuung an Ammoniumchlorid¶
In einem Raum wird eine Flasche mit Ammoniak conc. neben eine Flasche mit Salzsäure conc. Gestellt. Die Rauchbildung wird beobachtet. Danach wird abgelöscht und mit dem Laser auf eine Wand gestrahlt. Man sieht den Strahl nicht. Erst wenn man auch den Rauch strahlt, sieht man den Strahl, da der Strahl gestreut wird. Dabei wechselwirken die Schwebeteilchen in der Luft mit den Photonen und streuen sie in alle Raumrichtungen. Auf diese Weise können wir Lichtstrahlen aufnehmen (und so das Licht überhaupt sehen). Dabei geht dem Licht Energie in Strahlungsrichtung verloren.
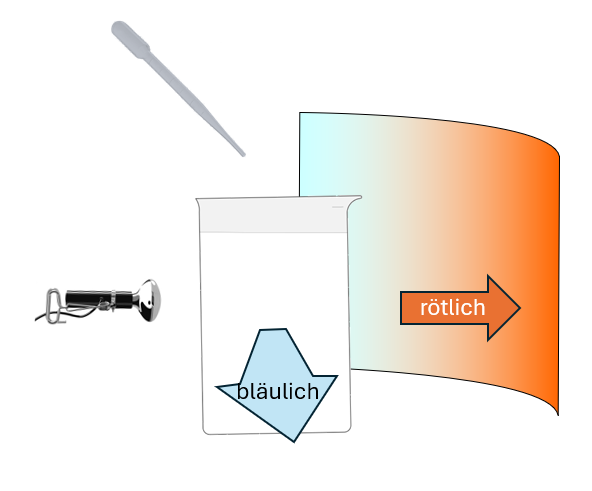
C.2 Vorrgehen: zuerst Vorderseite Licht und Farben, dann Streuung. Dann: werden alle Lichtquanten gleich gestreut? Experiment mit Milch. Es hat sich gezeigt: sobald die Körnchen, an denen Licht gestreut wird, kleiner als die Wellenlänge von Licht sind, werden Quanten umso stärker gestreut, je kürzer ihre Wellenlänge. Dann erklären, was von einem Sonnenstrahl, der fast horizontal viel Luft durchdringt, bei einem Beobachter ankommt (Rot der Abendsonne) und was ein Beobachter von dem Sonnenstrahl sieht, über den der Strahl hinweggeht (Blau des Himmels).¶
Becherglas mit Wasser füllen - Milch tropfenweise zugeben, umrühren - Mit Spotlampe durchzünden - Bei richtiger Milchkonzentration: Zur Seite kommt bläuliches, in Strahlrichtung rötliches Licht - Papier oder weisses Brett hinhalten als Bildschirm
Irrtum der Flat Earthers¶
Gedankenexperiment Wie sieht Michael aus, wenn man ihn neben die Erde im Weltraum schweben lässt. Der Sonne zugewandte Seite: hell und klar zu sehen, extrem scharfe Konturen. Der Sonne abgewandte Seite: unsichtbar! Denn auf die Rückseite trifft von nirgendwoher Licht, also kann auch kein Licht ins Auge des Betrachters gestreut / reflektiert werden. Michael wirkt praktisch wie eine der Sonne zugewandte Seite, die von hinten hohl ist! Warum ist das auf der Erde anders? Von hinten trifft auch Licht auf! Dieses stammt
- aus der Luft: an den Luftmolekülen gestreutes, Blaues Licht des Himmels trifft von allen Richtungen aus dem Himmel auf Michael. Weil dieses Licht auf dem Mond fehlt, sind die Schatten auf dem Mond schärfer als auf der Erde.
- Licht, das vom Boden und von anderen Oberflächen zu Michael reflektiert wird und von dort ins Auge des Betrachters.
Wenn man die dunkle, sonnenabgewandte Seite des Mondes doch sehen kann, so liegt dies am Licht, das von der Erde zum Mond reflektiert wird und von dort wiederum ins Auge des Betrachters. Das Licht der Sterne mag auch noch ein bisschen etwas dazu beitragen.
D. Farben durch Absorption¶
Material
D.1 Absorption von Licht durch Farbfilter¶
- Gleiche Ausrüstung wie A.1 Weisses Licht mit Gitter zerlegen
- Farbfilter (farbige durchsichtige Plättchen), um Bereiche des Farbschlitzes auf dem Hellraumprojektor abzudecken und die hindurchtretende Farbe zu untersuchen
D.2 Oberflächen reflektieren und absorbieren¶
- grüner und roter Pointer (
- Spotlampen unterschiedlicher Farben (auf z.B. rote Türe gerichtet / auf blaue Oberfläche gerichtet verändert sich die Helligkeit von rotem/blauem Licht unterschidlich.
- Mausefalle
D.3 Messung der Absorption im Photospektrometer¶
Pro Gruppe (oder wenigstens 2 mal)
- Mess-Laptop Chemie
- Photospektrometer Vernier
- Computer oder Mobiltelefon mit der nötigen Software (Hilfsmittel)
- Küvetten 3 mL (wie Posten 4)
- Farbige Lösungen mit Pipetten oder in Tropffläschchen:
- Phenolrot (für rot)
- Bromthymolblau, leicht basisch (für blau)
- Methylenblaulösung (für cyan)
- Inkjet gelb, magenta (bringt leis)
- Lugolsche Lösung (Iod / Kaliumiodid-Lösung)
- Pentan
D.4 Konzentrationsbestimmung eines Farbstoffes (z.B. Kristallviolett) mittels Photospektrometer¶
D.5 Photospektrometer selber bauen¶
- Lego-photospektrometer untersuchen und erklären
- Küvetten
- farbige LED-Spotlampe
- mit verschiedenen Farbfiltern (Um Frequenzen auszuwählen, anstelle des Gitters) oder mit einem Dioden-Rack vom Lego-Photospektrometer und einer mit Spannungsmessgerät verbundenen Solarzelle (als Detektor) selber ein rudimentäers Photospektrometer bauen.
Durchführung und Hinweise
D.1 Absorption von Licht durch Farbfilter¶
Wie viel Licht kommt durch, wenn man vor weisses oder rotes oder blaues Licht einen roten Farbfilter hält? Kann das auch Lichtstreuung sein? Nein, denn wo ist das fehlende Licht? Ds Plättchen wird mit der Zeit warm! Leuchtbox-Farbfilter und LED-Farbspots in allen Kombinationen testen. Am besten sind Unterschiede zu sehen, wenn ein Schrittzug im Inneren des Spot-Lampenschirms durch den Filter hindurch zu lesen ist.
Wie kann von Atomen absorbiertes Licht in Wärme umgewandelt werden? Eine gespannte Mausefalle (angeregtes Atom) wird aus sehr geringer Höhe auf eine Oberfläche fallen gelassen. Sie springt empor: Bei zusammenstössen schnappen die Elektronen der Atome zurück und dies gibt einen Rückstoss, Beschleunigung.
D.2 Oberflächen reflektieren und absorbieren¶
roten und grünen Farb-Laser auf unterschiedliche Oberflächen richten. Wann wird der Fleck besonders hell? Roter Laser auf roter Oberfläche, grüner Laser auf grüner! Wieso? Welchen Effekt haben Farbfilter?
D.3 Messung der Absorption im Photospektrometer¶
Photospektrometrie: Eine Tintenstrahlerdruckerfarbe auswählen lassen, Absorptionskurve vorhersagen lassen, dann Wellenlänge für Wellenlänge messen (Schritte von 50 bis 100 nm) und zeichnen lassen. Dann ganzes Spektrum fahren. Dann weitere Tintenstrahlerdrucker-Farbe dazugeben und Farbeindruck und Spektrum vorhersagen lassen, und schlussendlich mit der letzten Farbe wiederholen.
E. Absorption und Emission durch Atome¶
Material
E.1 Flammenfarben¶
- verdunkelbarer Raum
- Gasbrenner
- Magnesiastäbchen
- Konzentrierte Lösungen von Salzen: LiCl, NaCl, KCl, CaCl₂, CuCl₂, SrCl₂,
E.2 Atomspektren anschauen¶
- Gasentladungslampen He, Ne, Ar, mit (zur Erzeugung der Emissionsspektren von Elementen)
- Hochspannungs-Trafo
- Hand-Leuchtstoffröhre (Quecksilberdampf)
- Handspektrometer
E.3 Essiggurkenlampe mit Natriumlinien¶
- Handspektrometer
- eine ganze Essiggurke
- grosse Styroporplatte als Unterlage
- Mobiler FI-Schalter
- Hochspannungstrafo für leuchtende Essiggurke (besser als Strom von der Steckdose?)
- Anschlüsse für Trafo mit Krokodilklemmen und zwei grossen Nägeln (um Gurke anzuschliessen)
- Stativ und Klemme, um Kabel zu befestigen
- Porzellanteller
Durchführung und Hinweise
E.2 Atomspektren anschauen¶
Mit dem Handspektrometer betrachten: Normale weisse Glühlampe (Hellraumprojektor), Gasentladungslampen, Leuchtstoffröhren (teils sehr schöne Quecksilberlinien), evtl. Flammenfarben, Sonnenspektrum (auch bei Hochnebel etc sieht man Fraunhofer-Linien). Physik hat Gasentladungslampen mit Luft, CO2.
Besprechen, weshalb Moleküle keine Linienspektren aufweisen. Wenn π-Systeme bereits behandelt wurden: zeigen, wie die „Bahnen“ in Molekülen tatsächlich aussehen (Benzol: tiefstes MO des π-Systems) und dann das Molekül schwingen lassen: Bahnen veändern sich dauernd, also Energien, also Absorptionskurve breit statt Linienspektrum.
F. What color is it¶
Folgendes Gemisch
- 2.5 L deionisiertes Wasser
- 0.25 g Natriumhydrogencarbonat (pH muss neutral oder schwach alkalisch sein)
- 1.0 g of Natriumfluorescein
- 0.25 g Bromphenolblau
Im Durchlicht transparent und rot, von vorne belichtet (unter UV) intensiv grün, undurchsichtig.
- Kürbiskernöl (funktioniert gleich wie what colour is it-Flasche). Man sieht auch hier sehr schön, dass das absorbierte und das emittierte Licht nicht komplementär sind.
Durchführung und Hinweise
Quelle: Earles, T. T. (1994). What Color Is it?, J. Chem. Edu. 71 : 768-769.
Einee Flasche mit einer wässrigen Lösung von Fluorescein und Bromphenolblau zeigt verblüffende Farbeffekte: Bei Beleuchtung von vorne erscheint die Flasche völlig undurchsichtig und leuchtend grün. Bei Beleuchtung von hinten erscheint sie hingegen transparent und rot. Wie ist das möglich?
Erklärung
Bei Beleuchtung mit Blau/UV fluoresziert das Fluorescein hell grün. Es absorbiert zwar auch im grünen Bereich, aber nur wenig, und emittiert sehr viel mehr, wenn angeregt (hohe Quantenausbeute). Dringt das Licht tief in die Lösung ein, so werden die UV-blauen-grünen Anteile mit zunehmender Tiefe absorbiert, also alle Wellenlängen, die aus der Fluoreszenz stammen oder Fluoreszenz bewirken könnten. Es bleiben nur sehr langwellige Anteile übrig, also erscheint das Durchlicht rot.
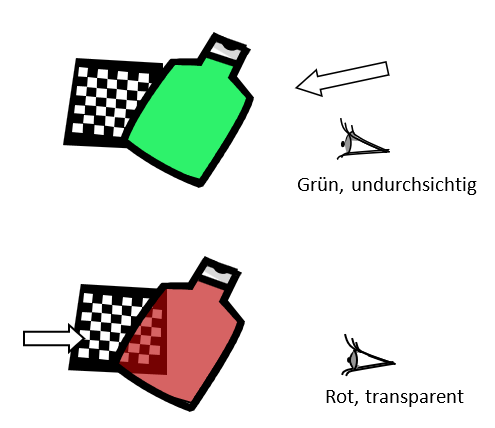
Eine genauere Untersuchung zeigt: die Flasche kann sogar grün erscheinen, wenn überhaupt kein grünes Licht eingestrahlt wird. Wird die Flasche beispielsweise im abgedunkelten Raum mit UV bestrahlt, so leuchtet sie grün. Aber auch bestrahlung mit violettem oder blauem Licht ergibt einen grünen Farbeindruck. Nur wenn mit grösseren Wellenlängen als 580 nm beleuchtet wird, erscheint die Flasche nicht grün.
a) Was passiert dabei und b) warum kann die Bestrahlung mit langwelligem, rotem Licht unmöglich zu einem grünen Leuchten führen?
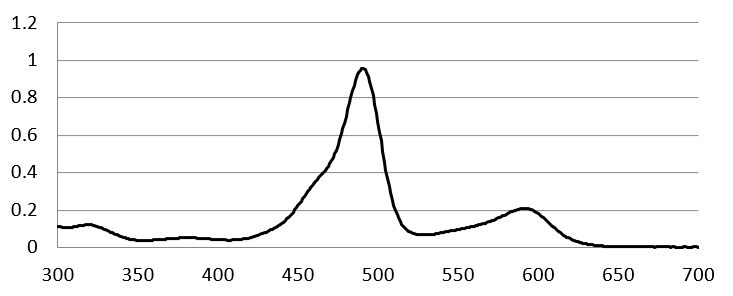
Erkläre mit Hilfe dieses Spektrums und der Erkenntnisse aus Aufgabe 1., warum die Flasche je nach Beleuchtung undurchsichtig grün oder transparent rot erscheint. Lösung zur what-color-is-it-Flasche
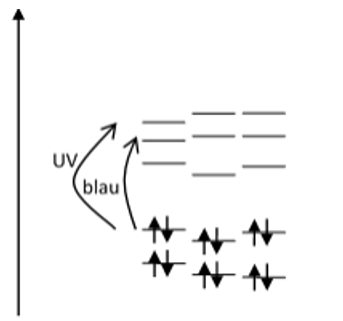
1a) Auch in Molekülen befinden sich Elektronen auf Bahnen. Die Bahnen im Farbstoffmoleküle Fluorescein könnten z.B. energetisch angeordnet sein, wie in der nebenstehenden Abbildung gezeigt: Es gibt besetzte Bahnen (unten, mit Doppelpfeilen) und leere Bahnen. Bei der Absorption eines Photons springt ein Elektron auf eine höhere Bahn. Die Bahnen liegen gerade so, dass UV, violette, blaue oder auch grüne Anteile des Lichtes anregen können. Beim zurückfallen wird die Energie entweder zur Wärme, oder dann wird IR oder grünes Licht frei (Auch UV oder blau können natürlich abgestrahlt werden, aber die Farbstoffmoleküle sind so konstruiert, dass v.a. grün abgestrahlt wird). Mit Hilfe eines solchen Moleküls wird UV und blaues Licht in grünes umgewandelt.
1b) Photonen von langwelligem, rotem Licht haben weniger Energie als diejenigen von grünem. Rotes Licht könnte den Elektronen also nicht auf eine genug hohe Bahn anregen, damit sie dann unter Aussendung von grünem Licht wieder in den Grundzustand zurückkehren können. 2. Wenn weisses Licht in die Flasche eindringt, so wird knapp unter der Oberfläche alles Licht mit Wellenlängen um 490 nm absorbiert und zu Wärme und grünem Licht umgewandelt (Bereich (1)). Denn in diesem Wellenlängenbereich absorbiert die Flüssigkeit ja gemäss Spektrum sehr gut. Das grüne Licht (500-560 nm) wird hingegen sehr viel weniger gut absorbiert. Vom reflektierten grünen Licht gelangt also viel zum Auge (A), dieses sieht die Flasche grün.
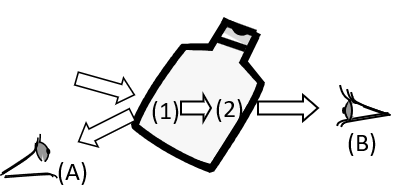
Das Licht, das in Richtung Auge (B) unterwegs ist, muss sehr viel Flüssigkeit durchqueren (2). Dabei werden die violetten, blauen und grünen Anteile des Spektrums alle verschluckt. Denn obwohl die Lösung in diesem Bereich teils nur schwach absorbiert, verschwinden die entsprechenden Wellenlängen doch fast vollständig, weil der Weg durch die Flüssigkeit so weit ist. Bei Auge (B) kommt dann nur noch rotes Licht an. Da dieses Licht aus einem Bereich hinter der Flasche stammt, erscheint die Flasche transparent. Warum nimmt das Auge (A) aber das rote Licht nicht wahr, das durch die Flasche hindurch kommt, warum erscheint die Flasche für Auge (A) undurchsichtig? Ganz einfach: die grüne Fluoreszenz ist so hell, dass für unser Auge das rote Licht, das durch die Flasche gelangt, völlig zugedeckt wird. Genau so, wie wir die Sterne tagsüber nicht leuchten sehen, weil der Himmel zu hell leuchtet. Könnte man das helle, grüne Licht wegfiltern, so würde das rote durchdringende Licht sichtbar.
Zum selber ausprobieren: Chlorophyll in Öl (bzw. Kürbiskernöl) zeigt ganz ähnliche Phänomene, nur dass dort die Fluoreszenz rot ist und die durchscheinende Farbe grün.
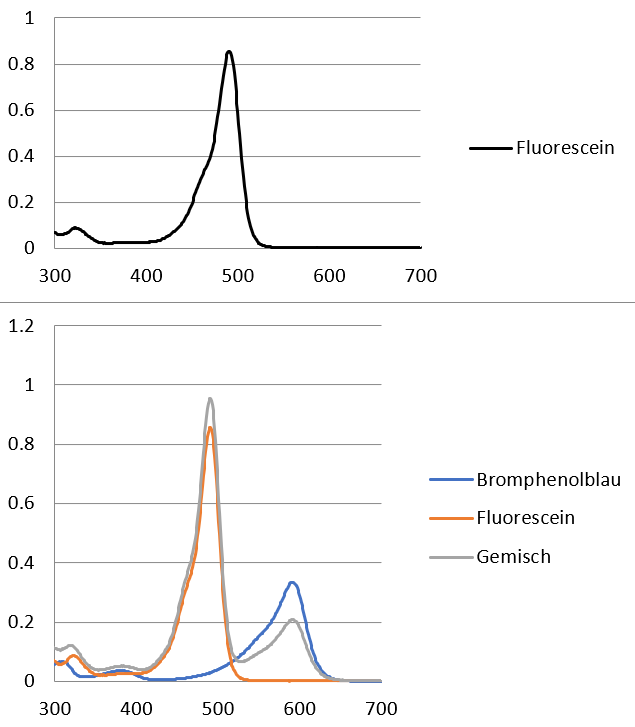
- Absorptionsmaximum: 485 nm (pH 9)
- Extinktionskoeffizient: 93 000 l·cm−1·mol−1 (pH 9)
- Emissionsmaximum: 514 nm (pH 9)
- Quantenausbeute: 0,93 (50 µmol Fluorescein in 0,1 mol Natriumboratpuffer, pH 9,5)
- Fluoreszenzlebensdauer: 4,16 ns (Dianion in Natronlauge)
Thomas T. Earles My chemistrv students and I have had some good discussions concerning a solution of fluorescein and Bromphenol blue. Such a solution has some rather interesting optical A properties. A fairly large quantity of solution is most effective, so I start with a clean 2.5-L reagent bottle and fill it with distilled water and then add 1.0 g of sodium fluorescein and 0.25 g of bromphenol blue and 0.25 g of sodium bicarbon ate. The solution must be neutral or slightly alkaline to get the desired colors. A good way to present the solution is to shine a lamp on it from one side in a darkened room and have the students file past it and look at it from both sides. Then ask them, 'What color is it?' On the light incident side it has a thick, green appearance; viewed from the other side it will be clear red. The students find this rather puzzling. Some even suspect that I've done something to color the glass on the inside of the bottle. So, What Calor Is It? The answer can be hven in terms of fluorescence and absorption. The fluorekein fluorrsct!~in the green reg~on of the spectrum. In othrr words, the blue-violet end of the spectrum and any ultraviolet light present are converted to green, so green is seen on the light incident side. The brompheuol blue absorbs the rest of the spectrum except red, so only red light is allowed to pass through the solution.If you pass white light through the solution and look at it through a spectroscope it will appear pure red. A pool of the solution poured onto a table top gives an impressive effect, especially when a UV lamp is used to illuminate it. This solution keeps indefinitely in a dark cabinet. While there are no specifich hazards with us in^ these chemicals students should be advised that stains to skin and clothing may result from contact. An Additional Activity Have students look up the dyes in the Merck Index for other properties and uses. Literature Cited 1. TheMerck In&, 11th ed., pp 21&219. 2. The Merck In&, p 651. Volume
G. Fluoreszenz, Phosphoreszenz, photochemische Reaktion und Chemilumineszenz¶
Material
F.1 Fluoreszenz und Phosphoreszenz¶
- UV-Leuchtstoffröhren
- UV-Taschenlampe
- Proben für UV-Leuchtstoffröhre
- Leuchtmarker
- RG mit fluoreszierendem Inhalt
- Geldschein, Pass, Kreditkarte, …
- Rosskastanienzweig (frisch schneiden und unter UV in Wasser einstellen)
- Zweig von einer Gewöhnlichen Mahonie (Mahonia aquifolium))
- Vollwaschmittel, optischer Aufheller
- Fluorit = Flussspat, CaF₂
- Fluoreszierende Schminke
- Fluoreszierender unsichtbarer Marker = UV-Stift
- Phosphoreszenz-Farbstoff (Slimy-Material)
- optional
- Schweppes
- durchsichtige Aperobächerli
- optional
- Trockeneis
F.2 Chlorophyll-Fluoreszenz¶
- verdunkelbarer Raum
- UV-Taschenlampe
- Chlorophyll-Extrakt in Aceton oder Diethylether (Kürbiskernöl verdünnen in Aceton) in Becherglas
F.3 Photochemische Reaktion¶
- UV-Taschenlampe oder -Lampe
- UV-Perlen
- Spiropyran-Folie (oder deren Herstellung)
F.4 Kalte Weissglut – Chemolumineszenz von Luminol mit KOH und DMSO¶
Gräte:
- 1 Liter - Erlenmeyerkolben [oder Messkolben, Rundkolben noch schöner] mit passendem Gummistopfen,
- Waage,
- Meßzylinder.
Chemikalien:
- festes Kaliumhydroxid (Kaliplätzchen) C,
- Dimethylsulfoxid (DMSO) Xi,
- Luminol.
- Fluoreszein (scheint eher zu quenchen, Fluorescum depuratum jedenfalls)
F.5 Phosphoreszenz und Fluoreszenz¶
- Fluoreszein-Natriumsalz
- Borsäure
- 200 mg Mononatriumsalz der 4-Amino-5-hy-droxynaphthalin-2,7-disulfonsäure* (sogenannte H-Säure)
- 3 große RG
- RG Klammer
- Wasserbad ca. 70 °C.
- UV-TaschenlampeLampe (λ = 366 nm) bzw.
Durchführung und Hinweise
F.2 Chlorophyll-Fluoreszenz¶
Durchführung: Chlorophyll erscheint im Auflicht grün, fluoresziert aber rot. Rot ist ungefähr die Komplementärfarbe des Grün (Komplementärfarbe würde Sinn machen). Da aber blaues Licht das Chlorophyll so anregt, dass es sofort nach rot de-exitiert wird, tritt blaue Fluoreszenz nie auf. Würden blau angeregte Zustände auch fluoreszeren, so wäre die Fluoreszenz magenta und somit genau die Komplementärfarbe der normalen grünen Farbe.s
F.4 Kalte Weissglut – Chemolumineszenz von Luminol mit KOH und DMSO¶
Bei dieser Variante der Luminol-Oxidation wirkt der Sauerstoff aus der Luft als Oxidationsmittel in stark alkalischem Medium (KOH) und in einem aprotischen Lösungsmittel Dimethylsulfoxid DMSO. Das Leuchten verstärkt sich erheblich, wenn man den Kolben kräftig schüttelt und kann mehrere Stunden gehalten werden. Eine Intensivierung des Leuchtens erreicht man auch durch Zugabe einer Spatelspitze Fluoreszein. In einen 1 Liter - Erlenmeyerkolben werden zu 70 g KOH - Plätzchen 60 ml DMSO gegeben und 0,1 g Luminol zugesetzt. Man verschließt den Erlenmeyerkolben mit einem passenden Stopfen und schüttelt kräftig um. Im Dunkeln beobachtet man zunächst nur ein helles, grünlichblaues Leuchten an der Oberfläche der Kaliplätzchen. Allmählich leuchtet nach kräftigem Schütteln auch der ganze Kolbeninhalt recht hell und lang anhaltend. Damit es zu Beginn gut leuchtet, braucht es recht viele Plätzchen (da nur deren Oberfläche leuchtet), daher die grosse Menge. Entsorgung: Die organische Reaktionslösung wird abgegossen und in einen Sammelbehälter für organische, nicht halogenierte Lösungsmittel entsorgt. Die KOH - Plätzchen können in dem verschlossenen Erlenmeyerkolben bis zu einem erneuten Einsatz verbleiben (unterm Abzug stehen lassen!). Literatur: H. Brandl in: D. Wöhrle, M. W. Tausch und W.-D. Stohrer "Photochemie - Konzepte, Methoden, Experimente", Wiley, VCH, Weinheim, Berlin, New York, Chichester, Brisbane, Singapore, Toronto, 1998 M. Tausch, H. Brandl: "Lichtbeteiligung bei chemischen Reaktionen" in MNU, 50, 206, (1997)
V1Untersuchen Sie Geldscheine, Kreditkarten, Ausweise und Leuchtgegenstände aus Bastel- und Spielzeugläden im Licht einer UV-Handlampe(λ = 366 nm und λ = 254 nm). Was geschieht jeweils beim Ausschaltender Lampe?
V2Lösen Sie in einem großen Rggl. eine kleine Spatelspitze Fluoreszein-Natriumsalz* in ca. 70 mL Wasser und betrachten Sie die Lösung im Lichteiner UV-Handlampe (λ = 366 nm). Was geschieht beim Ausschalten derLampe?
V3Halten Sie einen frisch angeschnittenen Kastanienzweig(Aesculus hip-pocastanum)in ein mit Wassers gefülltes 1-L-Becherglas, das mit der UV-Handlampe (λ = 366 nm) angestrahlt wird. Beobachten Sie das Gesche-hen an der Schnittstelle genau und rühren Sie dann mit dem Zweig imWasser.
V4Stellen Sie in Rggl. Lösungen von verschiedenen Vollwaschmitteln mitund ohne optische Aufheller her und verfahren Sie wie in V1.
V5Zerreiben Sie in zwei Mörsern a) 25mg Fluoreszein-Natriumsalzund 10 g Borsäure bzw. b) 200 mg Mononatriumsalz der 4-Amino-5-hy-droxynaphthalin-2,7-disulfonsäure (sogenannte H-Säure) und 10 g Bor-säure. Beschicken Sie mehrere (mindestens drei) große Rggl. ca. 2 cmhoch mit jeweils einer dieser Mischungen. Fixieren Sie jeweils ein Rggl. ineine Klemme, die Sie in der Hand halten, und erhitzen Sie das Gemischvorsichtig, bis es schmilzt. Verteilen Sie die Schmelze durch Drehen desRggl. möglichst auf die gesamte Innenfläche des Rggl. Lassen Sie eine derhergestellten Proben auf Raumtemperatur abkühlen, kühlen Sie eine zweiteim Gefrierfach auf ca. –5 °C und erwärmen Sie die dritte im Wasserbadauf ca. 70 °C. Untersuchen Sie zunächst die beiden Proben a) und b) mitRaumtemperatur im Licht der UV-Lampe (λ = 366 nm). Beobachten Sie genau, was beim Ausschalten der Lampe geschieht. Halten Sie dann jeweils zwei Proben gleicher Zusammensetzung a) bzw. b) gleichzeitig insLicht der Lampe und beobachten Sie den Unterschied beim Ausschaltender Lampe.
V6Der Boden eines 1-L-Erlenmeyerkolbens wird ca. 0,5 cm hoch mit Kaliumhydroxid -Plätzchen bedeckt. Es werden 1 mL Dimethylsulfoxid undeine kleine Spatelspitze Luminol* hinzugefügt. Dann wird durch Rotations-bewegungen des offenen Kolbens für eine gute Durchmischung gesorgt.Beobachtung?
V7Lösen Sie in 100 mL Wasser 0,5 g Natriumcarbonat und 2 g Natri-umhydrogencarbonat. Fügen Sie eine kleine Spatelspitze Luminol hinzuund schütteln Sie, bis es sich gelöst hat. Geben Sie noch je eine Spatel-spitze Kupfersulfat und Ammoniumcarbonat hinzu und schütteln Sieerneut. GießenSieschließlichimDunkeln1 mLWasserstoffperoxid-Lösung*,w= 30 %, hinzu. Beobachtung?
Ausw ertunga) Ordnen Sie die verschiedenen Leuchterscheinungen aus V1 bis V6 mit-hilfe von B3 den BegriffenFluoreszenz, PhosphoreszenzundChemolumi-neszenzzu und nennen Sie Gemeinsamkeiten und Unterschiede dieserLeuchterscheinungen.b) Nennen Sie ähnliche, Ihnen bekannte Leuchterscheinungen
X.1 Licht und Farbe anspruchsvolles Praktikum¶
Material
Posten 1
- Dioden-Rack (Lego-Photospektrometer) (bei Leis)
- USB-Ladegerät mit Ladebuchsen zum Anhängen der Dioden
- Pasco-Spektrometer mit Laptop (neue Serie)
- Lichtleiter (Glasfaserkabel) zu Pasco-Spektrometer
Posten 2:
- 3 LED-Spotlampen mit Farbumschaltgerät (funktionstüchtig!) an Stativen
- Weisse Platte (Prüfungs-Tafel)
Posten 4:
Bitte bereitstellen pro Klasse
- 2 Multimeter
Leis, pro Gruppe
- 1 Micro:bit
- 1 Inventor's Kit für
- Widerstand 10 kOhm
- Widerstand 47 Ohm
- Jumperkabel
- Leuchtdioden rot, orange, gelb, grün, blau, uv, ir vom Lego-Spektrometer (sehr helle Dioden, die sich nicht von normalen micro:bit-Pins, sondern nur vom 3V-Pin aus betreiben lassen.
- Photowiderstand
- Farbige durchsichtige Platten
- Lego
- Schwarze und transparente farbige Platten aus dem Set «Hellraum-Spektrometer»
Durchführung und Hinweise
Material
Durchführung und Hinweise



Sicherheit¶
Sicherheitshinweise
Weiteres¶
Infos
- Nanoo-Zugang: nanoo.tv/sso/waad/
- Zugangslink, Video, Metadaten