Quiz¶
Hilfsmittel¶
Stoffliste¶
Material
| Nr | Stoff | Code 1 | Code 2 |
|---|---|---|---|
| 1 | Aceton (Propanon) | AA | 104 |
| 2 | Aluminiumnitrat nonahydrat (1) | DF | 106 |
| 3 | Aluminiumoxid | AC | 113 |
| 4 | Ammoniumchlorid | AD | 125 |
| 5 | Äpfelsäure | AB | 119 |
| 6 | Butanon | DI | 174 |
| 7 | Calciumcarbonat | AE | 123 |
| 8 | Calciumchlorid Hexahydrat | AF | 105 |
| 9 | Calciumhydroxid | AG | 155 |
| 10 | Calciumnitrat | AH | 152 |
| 11 | Calciumsulfat | AJ | 114 |
| 12 | Cobalt(II)-chlorid (aq) 0.1 M LOESUNG | DO | 216 |
| 13 | Cyclohexan | BT | 130 |
| 14 | Cyclohexen | CQ | 175 |
| 15 | Dichlormethan | AK | 120 |
| 16 | DMSO (Dimethylsulfoxid) | AR | 128 |
| 17 | Eisen (Pulver) | AL | 118 |
| 18 | Eisen(II)-sulfat (aq) 0.1 M LOESUNG | EB | 217 |
| 19 | Eisen(III)-chlorid (aq) 0.1 M LOESUNG | DR | 213 |
| 20 | Eisen(III)-nitrat Nonahydrat | AM | 158 |
| 21 | Ethan-1,2-diamin (Ethylendiamin) (aq) | AV | 137 |
| 22 | Ethan-1,2-diamin (Ethylendiamin) (aq) 0.1 M LOESUNG | AU | 136 |
| 23 | Ethan-1,2-diol (Ethylenglycol) | AN | 166 |
| 24 | Ethanal | DL | 210 |
| 25 | Ethanol | AO | 116 |
| 26 | Ethansäure | AP | 100 |
| 27 | Ethansäure (aq) 1.0 M LOESUNG | DS | 179 |
| 28 | Ethansäureethylester | CR | 178 |
| 29 | Ethansäurepentylester | BA | 124 |
| 30 | Glucose (Traubenzucker) | BC | 109 |
| 31 | Harnstoff | BD | 172 |
| 32 | Heptan | BE | 160 |
| 33 | Hexan | BF | 111 |
| 34 | Hexanal | DH | 128 |
| 35 | Kaliumbromid | BR | 174 |
| 36 | Kaliumcarbonat | AQ | 127 |
| 37 | Kaliumchlorid | EC | 219 |
| 38 | Kaliumhexacyanoferrat(III) (aq) 0.1 M LOESUNG | DM | 212 |
| 39 | Kaliumhydroxid | EK | 135 |
| 40 | Kaliumiodid | EJ | 224 |
| 41 | Kaliumnitrat | BG | 150 |
| 42 | Kaliumpermanganat | DW | 132 |
| 43 | Kaliumsulfat | BH | 162 |
| 44 | Kaliumthiocyanat | BJ | 157 |
| 45 | Kupfer(I)-oxid | DV | 133 |
| 46 | Kupfer(II)-chlorid (aq) 0.1 M LOESUNG | DN | 214 |
| 47 | Kupfer(II)-chlorid Dihydrat | BK | 112 |
| 48 | Kupfer(II)-nitrat (aq) 0.1 M LOESUNG | EA | 215 |
| 49 | Kupfer(II)-sulfat Pentahydrat | BL | 165 |
| 50 | Magnesium | ED | 182 |
| 51 | Magnesiumchlorid Hexahydrat | DG | 126 |
| 52 | Magnesiumnitrat Hexahydrat | BQ | 173 |
| 53 | Mangan(II)-chlorid | EG | 134 |
| 54 | Mangan(IV)-oxid (Braunstein) | DT | 221 |
| 55 | Mannitol | BS | 176 |
| 56 | Methanol | BM | 110 |
| 57 | Methansäure | BN | 115 |
| 58 | Methansäure (aq) 1.0 M LOESUNG | EF | 180 |
| 59 | Milchsäure (2-Hydroxypropansäure) | CT | 211 |
| 60 | Naphthalin | BO | 167 |
| 61 | Natriumacetat | BP | 159 |
| 62 | Natriumcarbonat Decahydrat | CA | 171 |
| 63 | Natriumchlorid | CB | 161 |
| 64 | Natriumhydrogencarbonat | CC | 101 |
| 65 | Natriumhydrogenphosphat | EH | 222 |
| 66 | Natriumhydrogensulfat Monohydrat | CD | 156 |
| 67 | Natriumhydroxid | CE | 121 |
| 68 | Natriumphosphat Dodecahydrat | CF | 168 |
| 69 | Natriumsulfat Decahydrat | CG | 151 |
| 70 | Natriumsulfat wasserfrei | DP | 218 |
| 71 | Natriumsulfit | DU | 223 |
| 72 | Nickel(II)-nitrat | DK | 131 |
| 73 | Octadecansäure (Stearinsäure) | CH | 103 |
| 74 | Octan | EE | 181 |
| 75 | Octan-1-ol | CJ | 164 |
| 76 | Ölsäure (Octadec-9-ensäure) | CK | 154 |
| 77 | Pentan | CL | 122 |
| 78 | Propan-1,2-diol | AT | 177 |
| 79 | Propan-1-ol | CM | 163 |
| 80 | Propan-2-ol | CQ | 127 |
| 81 | Propansäure | CN | 108 |
| 82 | Saccharose | CO | 170 |
| 83 | Salicylsäure | CP | 102 |
| 84 | Silber | DA | 169 |
| 85 | Sudan III | DQ | 220 |
| 86 | Toluol | DB | 117 |
| 87 | Wasser | DC | 153 |
| 88 | Zink | DE | 107 |
| 89 | Zinn (Sn) | AS | 129 |
(1) Aluminium-Ionen ergeben mit Carbonat-Ionen komplizierte schwerlösliche Salze (z.B. Scarbroit Al5(OH)13(CO3)·5H2O). Diese Salze sind aber schlecht charakterisiert und ihre genaue Löslichkeit nicht bekannt, daher fehlen sie in der Tabelle mit schwerlöslichen Salzen
Vergeben:
Codes: AA bis AS, BA bis BR, CA bis CQ, DA bis DG Zahlen: 100 - 129, 150 - 175
A. Quizzes mit Löslichkeit, Siedepunkt, Fällungen (Ohne organische Nachweisreaktionen)¶
A.1 Quiz¶
Material
Je in einer kleinen Schottflasche (enghals) mit Rinnenspatel auf Papierserviette oder Pipette in kleinem Erlenmeyer
| Nr | Stoff | Code 1 | Code 2 |
|---|---|---|---|
| 1 | Calciumcarbonat | AE | 123 |
| 2 | Calciumchlorid Hexahydrat | AF | 105 |
| 3 | Eisen(III)-nitrat Nonahydrat | AM | 158 |
| 4 | Heptan | BE | 160 |
| 5 | Magnesiumchlorid Hexahydrat | DG | 126 |
| 6 | Magnesiumnitrat Hexahydrat | BQ | 173 |
| 7 | Natriumcarbonat Decahydrat | CA | 171 |
| 8 | Natriumhydroxid | CE | 121 |
| 9 | Natriumsulfat Decahydrat | CG | 151 |
| 10 | Pentan | CL | 122 |
| 11 | Propan-1-ol | CM | 163 |
Posten 1: Nachweisreagenzien in Tropfflaschen oder mit Pipette in Erlenmeyer
- Universalindikator-Lösung
- Natriumsulfat 1.0 M
- Silbernitrat 0.1 M
- Calciumnitrat 0.1 M
- Salzsäure 10%
- Natriumcarbonat 0.1 M
-
Natriumhydroxid 1.0 M
-
Filzstifte zum Beschriften der Glasgefässe
- ausreichend Reagenzgläser (Karton auf die Fensterbank stellen)
Entscheidend für diesen Versuch ist, dass Magnesiumsulfat gut wasserlöslich ist, während Calciumsulfat schlecht löslich ist.
Durchführung und Hinweise
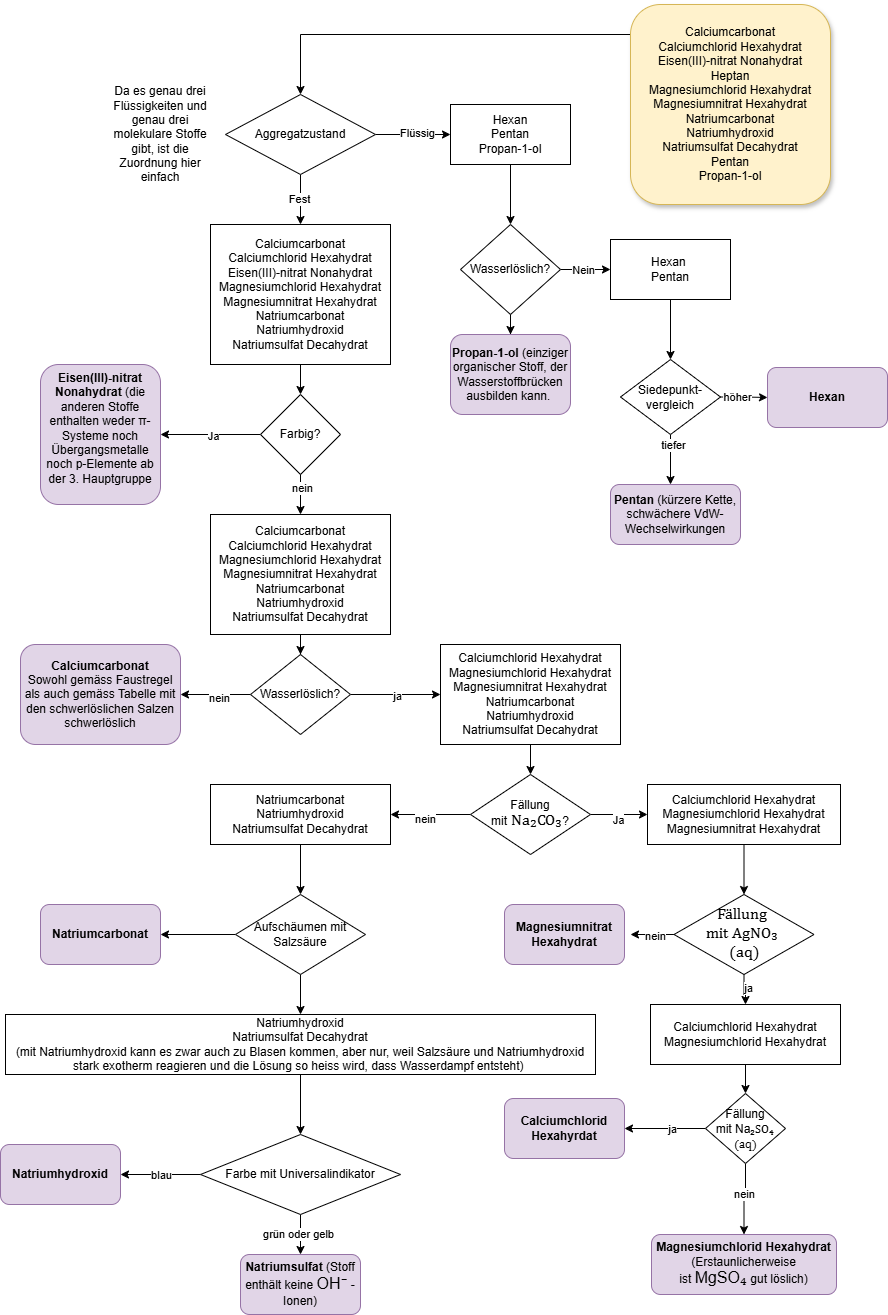
A.2 Quiz¶
Material
| Nr | Stoff | Code 1 | Code 2 |
|---|---|---|---|
| 1 | Calciumchlorid Hexahydrat | AF | 105 |
| 2 | Calciumhydroxid | AG | 155 |
| 3 | Calciumnitrat | AH | 152 |
| 4 | Eisenpulver | AL | 118 |
| 5 | Harnstoff | BD | 172 |
| 6 | Heptan | BE | 160 |
| 7 | Kupfer(II)-chlorid Dihydrat | BK | 112 |
| 8 | Kupfer(II)-sulfat Pentahydrat | BL | 165 |
| 9 | Methanol | BM | 110 |
| 10 | Naphthalin | BO | 167 |
| 11 | Natriumchlorid | CB | 161 |
| 12 | Natriumphosphat Dodecahydrat | CF | 168 |
| 13 | Pentan | CL | 122 |
| 14 | Propan-1-ol | CM | 163 |
| 15 | Salicylsäure | CP | 102 |
| 16 | Zink | DE | 107 |
Materialien:
- Leitfähigkeitsmessgerät (9V-Batterie, Diode,...)
- Magnet
- Wasserbad 95°C mit Deckel
- Filzstifte zum Beschriften der Glasgefässe
- ausreichend Reagenzgläser (Karton auf die Fensterbank stellen)
Tropfflaschen mit:
- Natriumcarbonat 0.1 M
- Silbernitrat 0.1 M
- Calciumnitrat 0.1 M
- Salzsäure 10%
- weitere im Glasschrank
B. OC-Nachweisreaktionen, ZMW, Fällungen (ohne Säure/Base, Komplex oder Redox)¶
B.1 Quiz Fällungen und OC-Nachweisreaktionen¶
Material
| Nr | Stoff | Code 1 | Code 2 |
|---|---|---|---|
| 5 | Calciumcarbonat | AE | 123 |
| 1 | Calciumchlorid | AF | 105 |
| 2 | Calciumhydroxid | AG | 155 |
| 3 | Calciumnitrat | AH | 152 |
| 4 | Eisenpulver | AL | 118 |
| 5 | Ethanol | AO | 116 |
| 6 | Heptan | BE | 160 |
| 7 | Kupfer(II)-sulfat Pentahydrat | BL | 165 |
| 8 | Naphthalin | BO | 167 |
| 9 | Natriumchlorid | CB | 161 |
| 10 | Octan-1-ol | CJ | 164 |
| 42 | Propansäure | CN | 108 |
| 11 | Zink | DE | 107 |
Materialien:
- Leitfähigkeitsmessgerät (9V-Batterie, Diode,...)
- Magnet
- Wasserbad 95°C mit Deckel
- Filzstifte zum Beschriften der Glasgefässe
- ausreichend Reagenzgläser (Karton auf die Fensterbank stellen)
Tropfflaschen mit:
- Natriumcarbonat 0.1 M
- Silbernitrat 0.1 M
- Calciumnitrat 0.1 M
- Salzsäure 10%
- weitere im Glasschrank
Posten 1: Cernitrattest:
- 40 g Cer(IV)-ammoniumnitrat in 100 mL Salpetersäure 2 M (pro Halbklasse 50 mL).
- Socorex 1 mL
- Socorex 2 mL
- Becherglas 500 mL
Posten 2: BTB-Reagenz:
- 0.02 g Bromthymolblau und 0.6 g NaOH in 100 mL Ethanol
- Socorex 1 mL
Durchführung und Hinweise
- Vorversuch: Kalk mit Salzsäure beträufeln
- Liste mit schwerlöslichen Salzen konsultieren
B.2 Quiz OC-Nachweisreaktionen und Fällungen¶
Material
| Nr | Stoff | Code 1 | Code 2 |
|---|---|---|---|
| 2 | Äpfelsäure | AB | 119 |
| 5 | Calciumcarbonat | AE | 123 |
| 6 | Calciumchlorid | AF | 105 |
| 9 | Calciumsulfat | AJ | 114 |
| 15 | Ethansäure | AP | 100 |
| 19 | Heptan | BE | 160 |
| 24 | Kupfer(II)-chlorid Dihydrat | BK | 112 |
| 25 | Kupfer(II)-sulfat Pentahydrat | BL | 165 |
| 26 | Methanol | BM | 110 |
| 30 | Natriumcarbonat Decahydrat | CA | 171 |
| 31 | Natriumchlorid | CB | 161 |
| 38 | Octan-1-ol | CJ | 164 |
| 40 | Pentan | CL | 122 |
| 49 | Aluminiumnitrat nonahydrat (1) | DF | 106 |
(1) Aluminium-Ionen ergeben mit Carbonat-Ionen komplizierte schwerlösliche Salze (z.B. Scarbroit Al5(OH)13(CO3)·5H2O). Diese Salze sind aber schlecht charakterisiert und ihre genaue Löslichkeit nicht bekannt, daher fehlen sie in der Tabelle mit schwerlöslichen Salzen
- Leitfähigkeitsmessgerät (9V-Batterie, Diode,...)
- Magnet
- Wasserbad 95°C mit Deckel
- Filzstifte zum Beschriften der Glasgefässe
- ausreichend Reagenzgläser (Karton auf die Fensterbank stellen)
Tropfflaschen mit:
- Natriumcarbonat 0.1 M
- Silbernitrat 0.1 M
- Calciumnitrat 0.1 M
- Salzsäure 10%
- weitere im Glasschrank
Posten 1: Cernitrattest:
- 40 g Cer(IV)-ammoniumnitrat in 100 mL Salpetersäure 2 M (pro Halbklasse 50 mL).
- Socorex 1 mL
- Socorex 2 mL
- Becherglas 500 mL
Posten 2: BTB-Reagenz:
- 0.02 g Bromthymolblau und 0.6 g NaOH in 100 mL Ethanol
- Socorex 1 mL
B.3 Chemie-Quiz Fokus: Organische Nachweise ohne Fehling- und nicht notwendig Iodoform-Test¶
Material
| Nr | Stoff | Code 1 | Code 2 |
|---|---|---|---|
| 1 | Aceton | AA | 104 |
| 2 | Ammoniumchlorid | AD | 125 |
| 3 | Calciumcarbonat | AE | 123 |
| 4 | Calciumchlorid Hexahydrat | AF | 105 |
| 5 | Calciumsulfat | AJ | 114 |
| 6 | Ethanol | AO | 116 |
| 7 | Ethansäurepentylester | BA | 124 |
| 8 | Harnstoff | BD | 172 |
| 9 | Heptan | BE | 160 |
| 10 | Milchsäure (2-Hydroxypropansäure) | CT | 211 |
| 11 | Natriumcarbonat Decahydrat | CA | 171 |
| 12 | Natriumchlorid | CB | 161 |
| 13 | Natriumhydroxid | CE | 121 |
| 14 | Natriumsulfat Decahydrat | CG | 151 |
| 15 | Octan-1-ol | CJ | 164 |
| 16 | Propansäure | CN | 108 |
Geräte¶
- Leitfähigkeitsmessgerät (9V-Batterie, Diode,...)
- Magnet
- Wasserbad 40°C mit Deckel für Rojahn keine Siedepunktbestimmung!
- Filzstifte zum Beschriften der Glasgefässe
- ausreichend Reagenzgläser (Karton auf die Fensterbank stellen)
Tropfflaschen mit:
- Natriumcarbonat 0.1 M
- Silbernitrat 0.1 M
- Calciumnitrat 0.1 M
- Salzsäure 10%
- weitere im Glasschrank
Organische Nachweisreaktionen¶
Siehe auch Organische Nachweisreaktionen
Posten 1: Cernitrattest: Bitte doppelt aufstellen¶
- 40 g Cer(IV)-ammoniumnitrat in 100 mL Salpetersäure 2 M (pro Halbklasse 50 mL).
- Socorex 1 mL
- Socorex 2 mL
- Becherglas 500 mL
Posten 2: Bayer-Probe 1: (wird hier eigentlich nicht gebraucht)¶
- Lösung I (0.1 g Kaliumpermanganat in 100 mL Wasser)
- Lösung III (Schwefelsäure 0.1 M).
- 2 Messzylinder 25 mL
- 1 Becherglas 100 mL
- Socorex 1 mL
Posten 3: BTB-Reagenz: Bitte doppelt aufstellen¶
- 0.02 g Bromthymolblau und 0.6 g NaOH in 100 mL Ethanol
- Tropfpipette
Posten 4: Rojahn-Test: (wird hier eigentlich nicht gebraucht)¶
- Ethanol mit Socorex 1 mL
- 1 Tropfflasche Phenolphthaleinlösung (0.1 g Phenolphthalein in 100 mL Ethanol)
- 100 mL NaOH 3 M mit Tropfpipette
Posten 5: Eisenchlorid-Test: (wird hier eigentlich nicht gebraucht)¶
- 1 Tropfflasche Phenolphthaleinlösung (0.1 g Phenolphthalein in 100 mL Ethanol)
- Salzsäure (0.5 M) mit Tropfpipette
- NaOH (3 M) mit Tropfpipettte
- Eisenchloridlösung (8 g FeCl₃ · 6 H₂O in 100 mL Wasser) mit Tropfpipette
- Pentan-1-ol (Amylalkohol) mit Tropfpipette
Posten 6: Iodoform-Probe Bitte doppelt aufstellen¶
- Iodreagenz (12.7 g Iod und 25.4 g Kaliumiodid mit Wasser auf 100 mL auffüllen) mit Tropfpipette
- 100 mL NaOH 3M mit Tropfpipette
B.4 kleiner Quiz und Aufgaben (Aldehyde Ketone Fehling Iodoform Spektren)¶
Material
| Nr | Stoff | Code 1 | Code 2 |
|---|---|---|---|
| 1 | Aceton | AA | 104 |
| 2 | Butanon | DI | 174 |
| 3 | Ethanal | DL | 210 |
| 4 | Propan-1-ol | CM | 163 |
| 5 | Propan-2-ol | CQ | 127 |
Geräte¶
- Wasserbad 95°C mit Deckel
- Filzstifte zum Beschriften der Glasgefässe
- ausreichend Reagenzgläser (Karton auf die Fensterbank stellen)
Schreibmaterial¶
- Schreibpapier
- Bleistifte und Kugelschreiber
- Lineale oder Geodreieck
Spektren (bringe ich selber)¶
Organische Nachweisreaktionen¶
Siehe auch Organische Nachweisreaktionen
Posten 1: Cernitrattest: Bitte doppelt aufstellen¶
- 40 g Cer(IV)-ammoniumnitrat in 100 mL Salpetersäure 2 M (pro Halbklasse 50 mL).
- Socorex 1 mL
- Socorex 2 mL
- Becherglas 500 mL
Posten 2: Bayer-Probe 1: (wird hier eigentlich nicht gebraucht)¶
- Lösung I (0.1 g Kaliumpermanganat in 100 mL Wasser)
- Lösung III (Schwefelsäure 0.1 M).
- 2 Messzylinder 25 mL
- 1 Becherglas 100 mL
- Socorex 1 mL
Posten 3: BTB-Reagenz: Bitte doppelt aufstellen¶
- 0.02 g Bromthymolblau und 0.6 g NaOH in 100 mL Ethanol
- Tropfpipette
Posten 4: Rojahn-Test: (wird hier eigentlich nicht gebraucht)¶
- Ethanol mit Socorex 1 mL
- 1 Tropfflasche Phenolphthaleinlösung (0.1 g Phenolphthalein in 100 mL Ethanol)
- 100 mL NaOH 3 M mit Tropfpipette
Posten 5: Eisenchlorid-Test: (wird hier eigentlich nicht gebraucht)¶
- 1 Tropfflasche Phenolphthaleinlösung (0.1 g Phenolphthalein in 100 mL Ethanol)
- Salzsäure (0.5 M) mit Tropfpipette
- NaOH (3 M) mit Tropfpipettte
- Eisenchloridlösung (8 g FeCl₃ · 6 H₂O in 100 mL Wasser) mit Tropfpipette
- Pentan-1-ol (Amylalkohol) mit Tropfpipette
Posten 6: Fehling Bitte doppelt aufstellen¶
- Fehling I (7 g CuSO₄ · 5 H₂O in 100 mL Wasser),
- Fehling II (35 g KNa-Tartrat und 10 g NaOH in 100 mL Wasser)
Posten 7: Iodoform-Probe Bitte doppelt aufstellen¶
- Iodreagenz (12.7 g Iod und 25.4 g Kaliumiodid mit Wasser auf 100 mL auffüllen) mit Tropfpipette
- 100 mL NaOH 3M mit Tropfpipette
B.20 Inverser Quiz LEISTUNGSERHEBUNG¶
Material
Chemikalien¶
- Universalindikator-Lösung
- Natriumsulfat 1.0 M
- Silbernitrat 0.1 M
- Salzsäure 10%
- Natriumcarbonat 0.1 M
- Natriumhydroxid 1.0 M
Geräte¶
- Wasserbad 95°C mit Deckel
- Analoge Thermometer (die SuS dürfen keinen Computer verwenden)
- Filzstifte zum Beschriften der Glasgefässe
- ausreichend Reagenzgläser (Karton auf die Fensterbank stellen)
Schreibmaterial¶
- Schreibpapier
- Bleistifte und Kugelschreiber
- Lineale oder Geodreieck
Organische Nachweisreaktionen¶
Siehe auch Organische Nachweisreaktionen
Posten 1: Cernitrattest:
- 40 g Cer(IV)-ammoniumnitrat in 100 mL Salpetersäure 2 M (pro Halbklasse 50 mL).
- Socorex 1 mL
- Socorex 2 mL
- Becherglas 500 mL
Posten 2: Bayer-Probe 1:
- Lösung I (0.1 g Kaliumpermanganat in 100 mL Wasser)
- Lösung III (Schwefelsäure 0.1 M).
- 2 Messzylinder 25 mL
- 1 Becherglas 100 mL
- Socorex 1 mL
Posten 3: BTB-Reagenz:
- 0.02 g Bromthymolblau und 0.6 g NaOH in 100 mL Ethanol
- Tropfpipette
Posten 4: Rojahn-Test:
- Ethanol mit Socorex 1 mL
- 1 Tropfflasche Phenolphthaleinlösung (0.1 g Phenolphthalein in 100 mL Ethanol)
- 100 mL NaOH 3 M mit Tropfpipette
Posten 5: Eisenchlorid-Test:
- 1 Tropfflasche Phenolphthaleinlösung (0.1 g Phenolphthalein in 100 mL Ethanol)
- Salzsäure (0.5 M) mit Tropfpipette
- NaOH (3 M) mit Tropfpipettte
- Eisenchloridlösung (8 g FeCl₃ · 6 H₂O in 100 mL Wasser) mit Tropfpipette
- Pentan-1-ol (Amylalkohol) mit Tropfpipette
Alles Weitere nach Bedarf
Durchführung und Hinweise
Aufgabe und Bewertung: Entwerft ein Identifikationsproblem und probiert aus, ob das von euch vorgesehene Schema funktioniert.
Abzugeben ist
- eine Liste mit Chemikalien, die zu identifizieren sind
- ein mögliches Vorgehen (kann stichwortartig oder schematisch erfolgen, muss aber klar nachvollziehbar sein).
- Beschriftete Fotos vom Versuch.
Anforderungen:
- Siedepunkte dürfen nicht verwendet werden.
- Die Identifikation soll nur möglich sein, wenn folgende Eigenschaften untersucht werden (oder andere vergleichbar anspruchsvolle):
- Löslichkeit in Wasser bzw. homogene Mischbarkeit
- Aggregatzustand bei Raumtemperatur
- Unterscheidung von Anionen mittels Fällungsreaktion. Vorsicht: wenn die Löslichkeitskonstante zu gross ist, etwa wie bei Silber(I)-sulfat, lässt sich oftmals mit den normalerweise verwendeten Konzentrationen keine Fällung beobachten.
- Unterscheidung von Kationen mittels Fällungsreaktion.
- Identifikation von Stoffen mittels pH der wässrigen Lösung.
- Identifikation eines Stoffes aufgrund seiner Fähigkeit zu puffern. Unter den Proben sollten also zwei Säuren oder zwei Basen vorkommen, wobei eine puffert und eine nicht.
- Identifikation eines Stoffes mittels Gasentwicklung (z.B. Carbonationen mit Salzsäure).
- Identifikation eines Stoffes mittels Rojahnprobe (Ester) oder Cernitratprobe (Alkohol).
Hilfsmittel
- Labor und Schlüssel zum Chemikalienschrank 😉. Vorgehen
- Entweder, ihr schaut die Unterlagen von letzter Woche nicht an. In diesem Fall könnt ihr für alle Chemikalien frei Vorschläge machen und ich ersetze dann diejenigen, die nicht vorhanden oder zu gefährlich sind.
- Falls ihr die Unterlagen von letzter Woche verwenden wollt, muss alles anders sein: Kein Stoff darf identisch sein, es müssen andere Kationen nachgewiesen werden, andere Anionen, andere potentielle Säuren und Basen, etc, und es muss ein anderer organischer Nachweis eingebaut werden.
B.21 Quiz LEISTUNGSERHEBUNG noch ohne Iodoform¶
Material
Konzept¶
- Organische Stoffe findet man über die Wasserlöslichkeit und die Nachweisreaktionen.
- Diejenigen Stoffe, die ansonsten in keinem Test reagieren, lassen sich mit der Bayer-Probe unterscheiden (Cyclohexen vs Heptan)
- Salze durch Fällungsreaktionen unterscheiden
Unbekannte Stoffe¶
| Nr | Stoff | Code 1 | Code 2 |
|---|---|---|---|
| 1 | Aceton | AA | 104 |
| 2 | Calciumcarbonat | AE | 123 |
| 3 | Calciumchlorid Hexahydrat | AF | 105 |
| 4 | Calciumsulfat | AJ | 114 |
| 5 | Eisenpulver | AL | 118 |
| 6 | Heptan | BE | 160 |
| 7 | Kupfer(II)-chlorid Dihydrat | BK | 112 |
| 8 | Octan-1-ol | CJ | 164 |
| 9 | Propan-1-ol | CM | 163 |
| 10 | Propansäure | CN | 108 |
| 11 | Kaliumcarbonat | AQ | 127 |
| 12 | Kaliumbromid | BR | 174 |
| 13 | Zinn (Sn) | AS | 129 |
| 14 | Cyclohexen | CQ | 175 |
Chemikalien¶
- Universalindikator-Lösung
- Natriumsulfat 1.0 M
- Silbernitrat 0.1 M
- Salzsäure 10%
- Natriumcarbonat 0.1 M
- Natriumhydroxid 1.0 M
Geräte¶
- Wasserbad 95°C mit Deckel
- Analoge Thermometer (die SuS dürfen keinen Computer verwenden)
- Filzstifte zum Beschriften der Glasgefässe
- ausreichend Reagenzgläser (Karton auf die Fensterbank stellen)
Schreibmaterial¶
- Schreibpapier
- Bleistifte und Kugelschreiber
- Lineale oder Geodreieck
Organische Nachweisreaktionen¶
Siehe auch Organische Nachweisreaktionen
Posten 1: Cernitrattest:
- 40 g Cer(IV)-ammoniumnitrat in 100 mL Salpetersäure 2 M (pro Halbklasse 50 mL).
- Socorex 1 mL
- Socorex 2 mL
- Becherglas 500 mL
Posten 2: Bayer-Probe 1:
- Lösung I (0.1 g Kaliumpermanganat in 100 mL Wasser)
- Lösung III (Schwefelsäure 0.1 M).
- 2 Messzylinder 25 mL
- 1 Becherglas 100 mL
- Socorex 1 mL
Posten 3: BTB-Reagenz:
- 0.02 g Bromthymolblau und 0.6 g NaOH in 100 mL Ethanol
- Tropfpipette
Posten 4: Rojahn-Test:
- Ethanol mit Socorex 1 mL
- 1 Tropfflasche Phenolphthaleinlösung (0.1 g Phenolphthalein in 100 mL Ethanol)
- 100 mL NaOH 3 M mit Tropfpipette
Posten 5: Eisenchlorid-Test:
- 1 Tropfflasche Phenolphthaleinlösung (0.1 g Phenolphthalein in 100 mL Ethanol)
- Salzsäure (0.5 M) mit Tropfpipette
- NaOH (3 M) mit Tropfpipettte
- Eisenchloridlösung (8 g FeCl₃ · 6 H₂O in 100 mL Wasser) mit Tropfpipette
- Pentan-1-ol (Amylalkohol) mit Tropfpipette
B.22 Quiz LEISTUNGSERHEBUNG (Aldehyde Ketone Fehling Iodoform Spektren)¶
Material
Anleitung im Voraus abgeben!
Konzept¶
- Neu sind Iodoform- und Fehlingprobe nötig für die Unterscheidung von Stoffen
- Zudem können gewisse Stoffe nur anhand ihrer Spektren unterschieden werden
- Bei den Salzen hilft es, wenn den SuS klar ist, welche Metallionen zu farbigen Salzen führen.
Unbekannte Stoffe¶
| Nr | Stoff | Code 1 | Code 2 |
|---|---|---|---|
| 1 | Aceton | AA | 104 |
| 2 | Dichlormethan | AK | 120 |
| 3 | Glucose | BC | 109 |
| 4 | Heptan | BE | 160 |
| 5 | Kupfer(II)-chlorid Dihydrat | BK | 112 |
| 6 | Natriumchlorid | CB | 161 |
| 7 | Pentan | CL | 122 |
| 8 | Propan-1-ol | CM | 163 |
| 9 | Kaliumcarbonat | AQ | 127 |
| 10 | Propan-1,2-diol | AT | 177 |
| 11 | Mannitol | BS | 176 |
| 12 | Cyclohexan | BT | 130 |
| 13 | Nickel(II)-nitrat | DK | 131 |
| 14 | Ethylacetat | CR | 178 |
Chemikalien¶
- Universalindikator-Lösung
- Natriumsulfat 1.0 M
- Silbernitrat 0.1 M
- Salzsäure 10% (zur Identifikation von Carbonaten)
- Natriumcarbonat 0.1 M
- Natriumhydroxid 1.0 M
Geräte¶
- Wasserbad 95°C mit Deckel
- Analoge Thermometer (die SuS dürfen keinen Computer verwenden)
- Filzstifte zum Beschriften der Glasgefässe
- ausreichend Reagenzgläser (Karton auf die Fensterbank stellen)
Schreibmaterial¶
- Schreibpapier
- Bleistifte und Kugelschreiber
- Lineale oder Geodreieck
Spektren (bringe ich selber)¶
Organische Nachweisreaktionen¶
Siehe auch Organische Nachweisreaktionen
Posten 1: Cernitrattest: Bitte doppelt aufstellen¶
- 40 g Cer(IV)-ammoniumnitrat in 100 mL Salpetersäure 2 M (pro Halbklasse 50 mL).
- Socorex 1 mL
- Socorex 2 mL
- Becherglas 500 mL
Posten 2: Bayer-Probe 1:¶
- Lösung I (0.1 g Kaliumpermanganat in 100 mL Wasser)
- Lösung III (Schwefelsäure 0.1 M).
- 2 Messzylinder 25 mL
- 1 Becherglas 100 mL
- Socorex 1 mL
Posten 3: BTB-Reagenz: Bitte doppelt aufstellen¶
- 0.02 g Bromthymolblau und 0.6 g NaOH in 100 mL Ethanol
- Tropfpipette
Posten 4: Rojahn-Test:¶
- Ethanol mit Socorex 1 mL
- 1 Tropfflasche Phenolphthaleinlösung (0.1 g Phenolphthalein in 100 mL Ethanol)
- 100 mL NaOH 3 M mit Tropfpipette
Posten 5: Eisenchlorid-Test:¶
- 1 Tropfflasche Phenolphthaleinlösung (0.1 g Phenolphthalein in 100 mL Ethanol)
- Salzsäure (0.5 M) mit Tropfpipette
- NaOH (3 M) mit Tropfpipettte
- Eisenchloridlösung (8 g FeCl₃ · 6 H₂O in 100 mL Wasser) mit Tropfpipette
- Pentan-1-ol (Amylalkohol) mit Tropfpipette
Posten 6: Fehling Bitte doppelt aufstellen¶
- Fehling I (7 g CuSO₄ · 5 H₂O in 100 mL Wasser),
- Fehling II (35 g KNa-Tartrat und 10 g NaOH in 100 mL Wasser)
Posten 7: Iodoform-Probe Bitte doppelt aufstellen¶
- Iodreagenz (12.7 g Iod und 25.4 g Kaliumiodid mit Wasser auf 100 mL auffüllen) mit Tropfpipette
- 100 mL NaOH 3M mit Tropfpipette
C. Zusätzlich mit Säure/Base-Reaktionen¶
C.1 Quiz¶
Material
| Nr | Stoff | Code 1 | Code 2 |
|---|---|---|---|
| Nr | Stoff | Code 1 | Code 2 |
| -----: | :---------------------------------------------------- | :--------- | ---------: |
| 1 | Calciumcarbonat | AE | 123 |
| 2 | Calciumchlorid Hexahydrat | AF | 105 |
| 3 | Calciumnitrat | AH | 152 |
| 4 | Calciumsulfat | AJ | 114 |
| 5 | Kaliumnitrat | BG | 150 |
| 6 | Natriumchlorid | CB | 161 |
Chemikalien¶
- Universalindikator-Lösung
- Natriumsulfat 1.0 M
- Silbernitrat 0.1 M
- Salzsäure 10% (zur Identifikation von Carbonaten)
- Natriumcarbonat 0.1 M
- Natriumhydroxid 1.0 M
Geräte¶
- Filzstifte zum Beschriften der Glasgefässe
- ausreichend Reagenzgläser (Karton auf die Fensterbank stellen)
C.2 Quiz¶
Material
| Nr | Stoff | Code 1 | Code 2 |
|---|---|---|---|
| 1 | Aluminiumoxid | AC | 113 |
| 2 | Ethanol | AO | 116 |
| 3 | Ethansäure (aq) 1.0 M LOESUNG | DS | 179 |
| 4 | Ethan-1,2-diamin (Ethylendiamin) (aq) 0.1 M LOESUNG | AU | 136 |
| 5 | Heptan | BE | 160 |
| 6 | Kaliumcarbonat | AQ | 127 |
| 7 | Kaliumhydroxid | EK | 135 |
| 8 | Kaliumiodid | EJ | 224 |
| 9 | Kaliumnitrat | BG | 150 |
| 10 | Kaliumsulfat | BH | 162 |
| 11 | Natriumhydrogensulfat Monohydrat | CD | 156 |
| 12 | Octan-1-ol | CJ | 164 |
| 13 | Ölsäure (Octadec-9-ensäure) | CK | 154 |
| 14 | Pentan | CL | 122 |
Chemikalien¶
- Universalindikator-Lösung
- Natriumsulfat 1.0 M
- Silbernitrat 0.1 M
- Salzsäure 10% (zur Identifikation von Carbonaten)
- Natriumcarbonat 0.1 M
- Natriumhydroxid 1.0 M
Geräte¶
- Wasserbad 95°C mit Deckel
- Analoge Thermometer (die SuS dürfen keinen Computer verwenden)
- Filzstifte zum Beschriften der Glasgefässe
- ausreichend Reagenzgläser (Karton auf die Fensterbank stellen)
C.3 Quiz¶
Material
| Nr | Stoff | Code 1 | Code 2 |
|---|---|---|---|
| 1 | Calciumsulfat | AJ | 114 |
| 2 | Eisen(III)-nitrat Nonahydrat | AM | 158 |
| 3 | Kaliumbromid | BR | 174 |
| 4 | Kaliumnitrat | BG | 150 |
| 5 | Kaliumcarbonat | AQ | 127 |
| 6 | Kupfer(II)-sulfat Pentahydrat | BL | 165 |
| 7 | Magnesiumchlorid Hexahydrat | DG | 126 |
| 8 | Magnesiumnitrat Hexahydrat | BQ | 173 |
| 9 | Natriumacetat | BP | 159 |
| 10 | Natriumcarbonat | CA | 171 |
| 12 | Natriumhydrogencarbonat | CC | 101 |
| 13 | Natriumhydrogensulfat Monohydrat | CD | 156 |
| 14 | Natriumhydroxid | CE | 121 |
| 15 | Natriumphosphat | CF | 168 |
| 16 | Natriumsulfat | CG | 151 |
| 17 | Octan | EE | 181 |
| 18 | Propan-1-ol | CM | 163 |
| 19 | Propansäure | CN | 108 |
Chemikalien¶
- Universalindikator-Lösung
- Natriumsulfat 1.0 M
- Silbernitrat 0.1 M
- Salzsäure 10% (zur Identifikation von Carbonaten)
- Natriumcarbonat 0.1 M
- Natriumhydroxid 1.0 M
Geräte¶
- Wasserbad 95°C mit Deckel
- Analoge Thermometer (die SuS dürfen keinen Computer verwenden)
- Filzstifte zum Beschriften der Glasgefässe
- ausreichend Reagenzgläser (Karton auf die Fensterbank stellen)
D. Zusätzlich mit Komplex-Reaktionen¶
D.1 Fällungen und Komplexe¶
Material
| Nr | Stoff | Code 1 | Code 2 |
|---|---|---|---|
| 1 | Ammoniumchlorid | AD | 125 |
| 2 | Calciumcarbonat | AE | 123 |
| 3 | Calciumchlorid Hexahydrat | AF | 105 |
| 4 | Calciumhydroxid | AG | 155 |
| 5 | Cobalt(II)-chlorid (aq) 0.1 M LOESUNG | DO | 216 |
| 6 | Eisen(II)-sulfat (aq) 0.1 M LOESUNG | EB | 217 |
| 7 | Eisen(III)-chlorid (aq) 0.1 M LOESUNG | DR | 213 |
| 8 | Methanol | BM | 110 |
| 9 | Heptan | BE | 160 |
| 10 | Kaliumchlorid | EC | 219 |
| 11 | Kaliumhexacyanoferrat(III) (aq) 0.1 M LOESUNG | DM | 212 |
| 12 | Kupfer(II)-chlorid (aq) 0.1 M LOESUNG | DN | 214 |
| 13 | Kupfer(II)-nitrat (aq) 0.1 M LOESUNG | EA | 215 |
| 14 | Natriumsulfat Decahydrat | CG | 151 |
| 70 | Natriumsulfat wasserfrei | DP | 218 |
| 15 | Octan-1-ol | CJ | 164 |
| 16 | Pentan | CL | 122 |
| 17 | Salicylsäure | CP | 102 |
| 18 | Sudan III | DQ | 220 |
Zwei mal:
- Bunsenbrenner mit Feuerzeug im Abzug
- elektrischer Thermometer (Thermofühler) Vernier
Pro Klasse: Die Konzentrationen der Lösungen dürfen auch höher sein als angegeben, aber nicht kleiner.
- Wasserbad (auf ca 95°C starten zu Beginn der Lektion)
- 1 Leitfähigkeits-Messgeräte für Lösungen
Folgende Lösungen sollen entweder im Glaskasten oder dann auf den Tischen bereitstehen, müssen aber noch nicht aus dem Glaskasten herausgeräumt werden.
- Tropffläschchen mit Silbernitrat 0.1 M
- Tropffläschchen mit Bariumchlorid 1 M
- Tropffläschchen mit Kaliumrhodanid 0.1 M
- Tropffläschchen mit frischen Natriumcarbonat 1 M
- Tropffläschchen mit Kaliumhexacyanoferrat(II) 0.1 M
- Tropffläschchen mit Kaliumhexacyanoferrat(III) 0.1M
- Tropffläschchen mit Universalindikator
- Natronlauge 1M mit Tropfpipette in Erlenmeyer
- Salzsäure 1M mit Tropfpipette in Erlenmeyer
- Pufferlösung pH 7 mit Tropfpipette in Erlenmeyer
- Ammoniak (conz) mit Tropfpipette in Erlenmeyer
Durchführung und Hinweise
- Ethan 1,2-diol ist hier die einzige wasserlösliche, nicht elektrisch leitfähige Flüssigkeit (alle anderen "wasserlöslichen" sind wässrige Lösungen). Könnte über die Komplexierung von Kupfer verifiziert werden (Organische Nachweise: Vicinale OH-Gruppen). Ergibt sich aber auch aus der Zähflüssigkeit und dem hohen Siedepunkt.
E. Alle Reaktionstypen¶
E.1 Quiz 3¶
Material
| Nr | Stoff | Code 1 | Code 2 |
|---|---|---|---|
| 1 | Ammoniumchlorid | AD | 125 |
| 2 | Calciumchlorid Hexahydrat | AF | 105 |
| 3 | Calciumhydroxid | AG | 155 |
| 4 | Calciumnitrat | AH | 152 |
| 5 | Eisen (Pulver) | AL | 118 |
| 6 | Ethansäure (aq) 1.0 M LOESUNG | DS | 179 |
| 7 | Glucose (Traubenzucker) | BC | 109 |
| 8 | Harnstoff | BD | 172 |
| 9 | Magnesium | ED | 182 |
| 10 | Methansäure (aq) 1.0 M LOESUNG | EF | 180 |
| 11 | Natriumacetat | BP | 159 |
| 12 | Natriumchlorid | CB | 161 |
| 13 | Octan | EE | 181 |
| 14 | Ölsäure (Octadec-9-ensäure) | CK | 154 |
| 15 | Pentan | CL | 122 |
Ethan wird nicht aufgestellt
Zudem bitte bereitstellen::
- elektrischer Thermometer (Thermofühler) Vernier
- Wasserbad (auf ca 95°C starten zu Beginn der Lektion)
E.2 Quiz 4¶
Material
| Nr | Stoff | Code 1 | Code 2 |
|---|---|---|---|
| 1 | Ammoniumchlorid | AD | 125 |
| 2 | Calciumchlorid Hexahydrat | AF | 105 |
| 3 | Calciumhydroxid | AG | 155 |
| 4 | Eisen (Pulver) | AL | 118 |
| 5 | Eisen(II)-sulfat (aq) 0.1 M LOESUNG | EB | 217 |
| 6 | Eisen(III)-nitrat Nonahydrat | AM | 158 |
| 7 | Ethan-1,2-diol (Ethylenglycol) | AN | 166 |
| 8 | Ethansäure | AP | 100 |
| 9 | Glucose (Traubenzucker) | BC | 109 |
| 10 | Harnstoff | BD | 172 |
| 11 | Heptan | BE | 160 |
| 12 | Kaliumchlorid | EC | 219 |
| 13 | Kaliumhydroxid | EK | 135 |
| 14 | Kaliumpermanganat | DW | 132 |
| 15 | Kaliumthiocyanat | BJ | 157 |
| 16 | Natriumhydrogensulfat Monohydrat | CD | 156 |
| 17 | Octan-1-ol | CJ | 164 |
| 18 | Ölsäure (Octadec-9-ensäure) | CK | 154 |
| 19 | Pentan | CL | 122 |
| 20 | Zink | DE | 107 |
Zudem bitte bereitstellen:
- elektrischer Thermometer (Thermofühler) Vernier
- Wasserbad (auf ca 95°C starten zu Beginn der Lektion)
E.3 Quiz 5 (mit Wohl und Lahe plus Mannitol)¶
Material
| Nr | Stoff | Code 1 | Code 2 |
|---|---|---|---|
| 1 | Ammoniumchlorid | AD | 125 |
| 2 | Calciumchlorid Hexahydrat | AF | 105 |
| 3 | Calciumhydroxid | AG | 155 |
| 4 | Cyclohexen | CQ | 175 |
| 5 | Eisen (Pulver) | AL | 118 |
| 6 | Eisen(III)-nitrat Nonahydrat | AM | 158 |
| 7 | Ethan-1,2-diol (Ethylenglycol) | AN | 166 |
| 8 | Ethansäure | AP | 100 |
| 9 | Glucose (Traubenzucker) | BC | 109 |
| 10 | Harnstoff | BD | 172 |
| 11 | Heptan | BE | 160 |
| 12 | Kaliumchlorid | EC | 219 |
| 13 | Kaliumhydroxid | EK | 135 |
| 14 | Kaliumnitrat | BG | 150 |
| 15 | Kaliumsulfat | BH | 162 |
| 16 | Kaliumthiocyanat | BJ | 157 |
| 17 | Mannitol | BS | 176 |
| 18 | Octadecansäure (Stearinsäure) | CH | 103 |
| 19 | Octan-1-ol | CJ | 164 |
| 20 | Ölsäure (Octadec-9-ensäure) | CK | 154 |
| 21 | Pentan | CL | 122 |
| 22 | Silber | DA | 169 |
| 23 | Zink | DE | 107 |
Zudem bitte bereitstellen:
- elektrischer Thermometer (Thermofühler) Vernier
- Wasserbad (auf ca 95°C starten zu Beginn der Lektion)
E.4 Quiz 6¶
Material
| Nr | Stoff | Code 1 | Code 2 |
|---|---|---|---|
| 1 | Aceton (Propanon) | AA | 104 |
| 2 | Aluminiumoxid | AC | 113 |
| 3 | Cyclohexen | CQ | 175 |
| 4 | Eisen (Pulver) | AL | 118 |
| 5 | Eisen(III)-chlorid (aq) 0.1 M LOESUNG | DR | 213 |
| 6 | Eisen(III)-nitrat Nonahydrat | AM | 158 |
| 7 | Ethanol | AO | 116 |
| 8 | Ethansäure | AP | 100 |
| 9 | Heptan | BE | 160 |
| 10 | Kaliumpermanganat | DW | 132 |
| 11 | Kaliumiodid | EJ | 224 |
| 12 | Kaliumsulfat | BH | 162 |
| 13 | Kupfer(I)-oxid | DV | 133 |
| 14 | Kupfer(II)-chlorid Dihydrat | BK | 112 |
| 15 | Mangan(IV)-oxid (Braunstein) | DT | 221 |
| 16 | Natriumchlorid | CB | 161 |
| 17 | Natriumhydrogencarbonat | CC | 101 |
| 18 | Natriumhydrogensulfat Monohydrat | CD | 156 |
| 19 | Natriumsulfit | DU | 223 |
| 20 | Octan-1-ol | CJ | 164 |
| 21 | Octadecansäure (Stearinsäure) | CH | 103 |
| 22 | Ölsäure (Octadec-9-ensäure) | CK | 154 |
| 23 | Pentan | CL | 122 |
| 24 | Propan-1-ol | CM | 163 |
| 25 | Silber | DA | 169 |
| 26 | Sudan III | DQ | 220 |
| 27 | Zinn (Sn) | AS | 129 |
Butansäure wird nicht aufgestellt
Zudem bitte bereitstellen:
- elektrischer Thermometer (Thermofühler) Vernier
- Wasserbad (auf ca 95°C starten zu Beginn der Lektion)
- Frisches Chlorwasser