1. Kern, Hülle und Periodensystem¶
Material, Chemikalien und Hinweise¶
A. Elementarteilchen¶
Material
A.1 Materie besteht aus geladenen Teilchen¶
- Induktionsmaschine
- Kristallzucker
- Kristallzuckerwürfel
- Stabmixer elektrisch (ausprobieren!)
- Kaffeemühle elektrisch
- Methylsalicylsäure
- Pipetten
- Lifesavers



A.2 Elektronen im Kathodenstrahlrohr¶
- Kathodenstrahlröhre
- Hochspannungsquelle und -kabel mit Krokodilklemmen
- Hufeisenmagnet
- Laserpointer (um zu zeigen, dass Licht nicht abgelenkt wird)
A.3 Kanalstrahlrohr¶
- Kanahlstrahlrohr
- Hochspannungsquelle und Hochspannungskabel mit Krokodilklemmen
- Hufeisenmagnet (um zu zeigen, dass die Teilchen viel weniger stark abgelenkt werden)
Durchführung und Hinweise
A.1 Materie besteht aus geladenen Teilchen¶
Zucker mit Mehylsalicylsäure tränken (soll aber noch nicht zerfliessen) und in einen Standzylinder geben, in dem man den Zucker mit dem Stabmixer rühren kann. (Auch beim ZErquetschen mit dem Spatel von präparierten Zuckerwürfeln ist die Tribolumineszenz zu sehen (Gut geht es mit der Kaffeemühle, aber deren Kunststoffabdeckung löst sich im Methylsalicylat auf) Zimmer abdunkeln und Adaption abwarten, Stabmixer einstellen und mahlen. Der Zucker zeigt helle Tribolumineszenz, also unzählige kleine Blitzchen.
Selbstversuch: in einem völlig dunklen Zimmer vor dem Spiegel mit offenem Mund einen Lifesaver zerbeissen. Man sieht genau dieselben Blitzchen. Man kann solche Lollies auch zahnschonender mit Hammer oder Zange zerkleinern, wobei ein ziemlich heller blaugrüner Lichtblitz zu beobachten ist.
Mit der Influenzmaschine gelingt es, Kugeln elektrisch so stark aufzuladen, bis Blitze entstehen. Diese Blitze entstehen, weil negative Ladungsträger, also Elektronen, von der negativ geladenen Kugel zur positiven hüpfen (und gegen Moleküle in der Luft prallen). Genau dieselben Blitze entstehen auch, wenn man Moleküle zerschmettert. Ein Hinweis, dass in allen Molekülen dieselben geladenen Teilchen, also auch Elektronen, drin sein könnten. Beim Zerschlagen der Moleküle entstehen geladene Bruchstücke. Sobald der Abstand genug gross wird, wird stellenweise eine Durchschlagsspannung erreicht und es schlagen Blitze durch. Dabei werden die Luftmoleküle unter Farberscheinung ionisiert und angeregt (man kann zeigen, dass die Lichtblitze mindestens teilweise von angeregtem Stickstoff stammen).
Sehr feine Tribolumineszenz erreicht man auch - durch Abrollen von Klebestreifen (dabei wird sogar Röntgenstrahlung erzeugt!) oder selbstklebenden Briefumschlägen - In einem völlig abgedunkelten Raum reibt man mit einem Glasstab von innen an den Wänden eines Reagenzglases, das etwas zur Hälfte mit Haushaltszucker gefüllt ist. Während des Reibens kann man deutliche, weisse Lichtblitze wahrnehmen.
A.2 Elektronen im Kathodenstrahlrohr¶
Kathodenstrahlröhre Nanoo Meta https://nanoo.tv/link/b/1065241 | Zugangslink
B. Rutherford¶
Material
Nur Animationen
Durchführung und Hinweise
Siehe Videos und Animationen
C. Isotope¶
Material
- extrem verdunkelbarer Raum
- leuchtende Tritium-Probe (leuchtender winziger Schlüsselanhänger)
Siehe auch Videos und Animationen
Durchführung und Hinweise
D. Entstehung der Atome¶
Material
Video Timelapse of the entire universe siehe Videos und Animationen.
Durchführung und Hinweise
E. Radioaktivität¶
Material
- Kiste Leis mit Geigerzähler
- Radioaktive Proben
- Stein aus dem Wallis
- Glühstrumpf für Gaslampen
Durchführung und Hinweise
- Exkursion ins KKW
F. Schalenmodell¶
Material
Keine Versuche
Durchführung und Hinweise
G. Edelgase¶
Material
G.1 Edelgase sind harmlos¶
- Heliumflasche zum Einatmen und singen.
- Siehe Videos zu Krypton, Xenon, SF₆
G.2 Edelgase schützen¶
- Herkömmliche Glühlampe (Velolämpchen) in Fassung
- Tuch, Zange, Hammer und Glasschneider zum Knacken der Birne
- passende Spannungsquelle
- Glocke zum Füllen mit Helium
Durchführung und Hinweise
G.1¶
SuS auf Stuhl setzen, soll extrem tief ausatmen und dann tief einatmen, sobald der heliumstrahl einsetzt und danach reden oder singen (bitte vorher überlegen, was gesagt oder gesunden werden soll. Effekt hält nicht lange). LP öffnet den Heliumstrahl, sobald SuS ausgeatmet hat.
G.2¶
- Birne zum Öffnen in Tuch wickeln.
- Glühbirne wird unter der Glocke mit Helium betrieben. Sobald die Glocke entfernt wird, löst sich der Glühfaden in Rauch auf und das Glühen endet.
- Videos Schutzgasschweissen siehe Videoverzeichnis
H. Alkali- und Erdalkalimetalle: Reaktion mit Wasser¶
Material
G.1 Lithium reagiert mit Wasser¶
- 3 Reagenzgläser, RG-Ständer
- Feuerzeug
- Lithium-Draht
- NaCl (0.1 M)
- NaOH (0.1 M)
- Phenolphthalein-Indikatorlösung in Tropfflasche
- Glasplatte zum Schneiden
- Messer
- zwei grosse Pinzetten zum Herausholen und Manipulieren des Lithium-Drahtes.
G.2 Natrium reagiert mit wasser¶
- Grosse Glaswanne (z.B. Gratin-Form oder Riesen-Kristallisierschale)
- Natriumwürfel in Petrol
- Phenolphthalein-Indikatorlösung in Tropfflasche
- Glasplatte zum Schneiden
- Messer
- zwei grosse Pinzetten zum Herausholen und Manipulieren des Lithium-Drahtes.
- Hand-Geschirrspülmittel
- Splitterschutzscheibe mit Abdeckung (Prüfungswand)
G.3 Magnesium reagiert mit Wasser¶
- Magnestiumstreifen
- Deionisiertes Wasser
- Phenolphthalein-Indikatorlösung in Tropfflasche
Durchführung und Hinweise
- Mit Hilfe zweier RG plausibel machen, dass Phenolphthalein die Präsenz von OH⁻ anzeigt (einziger Unterschied zwischen NaOH (aq) und NaCl(aq))
- Beim Anschneiden der grauen Lithium-Drähte erscheint eine typisch metallisch glänzende Oberfläche.
- Zeigen, dass Lithium mit Wasser zu OH⁻ reagiert und unter Gasentwicklung
- Reaktiongleichung der Reaktion von Lithium mit Wasser plausibel machen:
- Das OH⁻ besteht aus O- und H-Atomen und muss daher aus Wassermolekülen entstehen. Die Wassermolekülen müssen dabei Wasserstoffatom verlieren und eine negative Ladung erhalten
- Die negative Ladung kann vom Lithium kommen. Wir wissen bereist, dass Lithium-Atome ihre Elektronen nur schwach festhalten.
- Es bleibt einzig ein H-Atom übrig, es sollte also auch Wasserstoff entstehen (wenn die Reaktion einigermassen einfach ist)
- Wasserstoff sollte sich nachweisen lassen: ist brennbar.
- Es wird die Flammenfarbe von Lithum sichtbar!
-
Die Reaktionsgleichung ergibt sich aus der Tatsache, dass die Gesamtladung der Edukte gleich sein muss wie die Gesamtladung der Produkte.
-
Wir nun Natrium heftiger oder weniger heftig reagieren? Wir vermuten: heftiger, da die Elektronen in Natrium schwächer festgehalten werden.
- Eine grosse Schale wird dünn mit Wasser gefüllt, mit tüchtig Phenolphthalein versetzt und mit einem Tropfen Spülmittel (damit das Natrium nicht an der Wand klebenbleibt)
- Ein Natriumstück wird allseitig von der Natriumoxid-Schicht befreit. Wieder erscheint eine typisch metallisch glänzende Oberfläche.
- Das Stück wird hiner der Splitterschutscheibe aufs Wasser geworfen, oben auf der Splitterschutzscheibe liegt ein Deckel so, dass allfällig esplodierendes Natriumperoxid nicht zu den SuS gelangen kann, auch wenn es nach oben wegspritzt.
- Das Metall hat so geringe Dichte, dass es schwimmt.
- wieder zischt es, hinter dem Metall ergibt sich eine rote Spur von gebildetem OH⁻
- Das Metall wird bei der Reaktion so heiss, das es schmilzt.
-
Splitterschutzscheibe gut waschen, sonst bleibt sie trüb.
-
Versuch wiederholen, aber diesmal ein Filterpapier auf das Wasser legen zur Immobilisierung des Natriumbällchens
- Nun beginnt das Natrium sogar zu brennen.
Rubidium, Cesium, Francium: Videos
Hinweis: Die verschiedenen Enthalpien im Zusammenhang mit der Reaktion sind:
| Atomsorte | ΔHᵣ | ΔSᵣ | ΔGᵣ | ΔH_hydr | Ionsierungsenergie | Ionsierungsenergie | ΔH_vap | Summe(Vap+Ioni+Hydr) | Summe - ΔHᵣ |
|---|---|---|---|---|---|---|---|---|---|
| [kJ/mol] | [J/mol/K] | [kJ/mol] | [kJ/mol] | eV | [kJ/mol] | [kJ/mol] | [kJ/mol] | [kJ/mol] | |
| Li | -533.336 | -299.88 | -443.93 | -508 | 5.39 | 520.0481229019999 | 159.3 | -343.31 | 190.026 |
| Na | -456.336 | -253.08 | -380.88 | -398 | 5.14 | 495.927152452 | 109 | -283.86 | 172.476 |
| K | -478.336 | -191.88 | -421.13 | -314 | 4.34 | 418.740047012 | 89 | -220.66 | 257.676 |
| Rb | -478.736 | -179.08 | -425.34 | -289 | 4.18 | 403.3026259239999 | 80.9 | -203.92 | 274.816 |
| Cs | -492.936 | -172.68 | -441.45 | -256 | 3.89 | 375.322300202 | 76.5 | -175.61 | 317.326 |
| Mg | -443.336 | -439.48 | -312.305 | -1908 | 7.64 | 737.1368569519999 | |||
| Fr | 4.07 | 392.68939892599997 |
Der Trend der Ionisierungsenergien stimmt also genau mit der Theorie überein - das ist das Wichtigste, denn darauf bezieht sich die Theorie ja, alle anderen Effekte sind nicht berücksichtigt. Ausnahme: Francium, allerdings lässt sich das mit der komplizierten inneren Struktur und fehlenden Messungen entschuldigen.
Bezüglich Reaktionsenthalpie zeigt sich derselbe Trend - abgesehen von Lithium, das sogar die höchste Reaktionsenthalpie von allen aufweist. Dies hängt mit der aussergewöhnlich hohen Hydratationsenthalpie zusammen (die Bildung der Ionen ist so günstig, weil sie durch Wasser so gut stabilisiert werden). Dennoch reagiert Lithium am wenigsten heftig - wohl, weil es aufgrund seiner geringen Dichte auf einem Gasfilm aus Wasserstoff schwebt und dies besser als Natrium. Die sehr heftige Reaktion von Rubidium und Cäsium dürfte vor allem damit zu tun haben, dass nur diese zwei dichter sind als Wasser und daher im Wasser versinken. Die Unterschiede der Reaktionsenthalpien wären wohl zu klein, um die stark unterschiedlichen Reaktivitäten zu erklären.
H. Halogene¶
Material
Filme siehe Videos
H.1 Herstellung von Chlorgas (Zylinder mit sandbedecktem Boden)¶
- Apparatur zur Herstellung von Chlorgas (oder je nach Bestellung bereits chlorgasgefüllten Zylinder, der mit gut gefettetem Deckel verschlossen ist)
- Kaliumpermanganat mit Polylöffel (3-4 Löffel)
- Konzentrierte Salzsäure
- Sand für in den Standzylinder
- Standzylinder mit sandbedecktem Boden und passendem, gefettetem Deckel
- Latex-Handschuhe
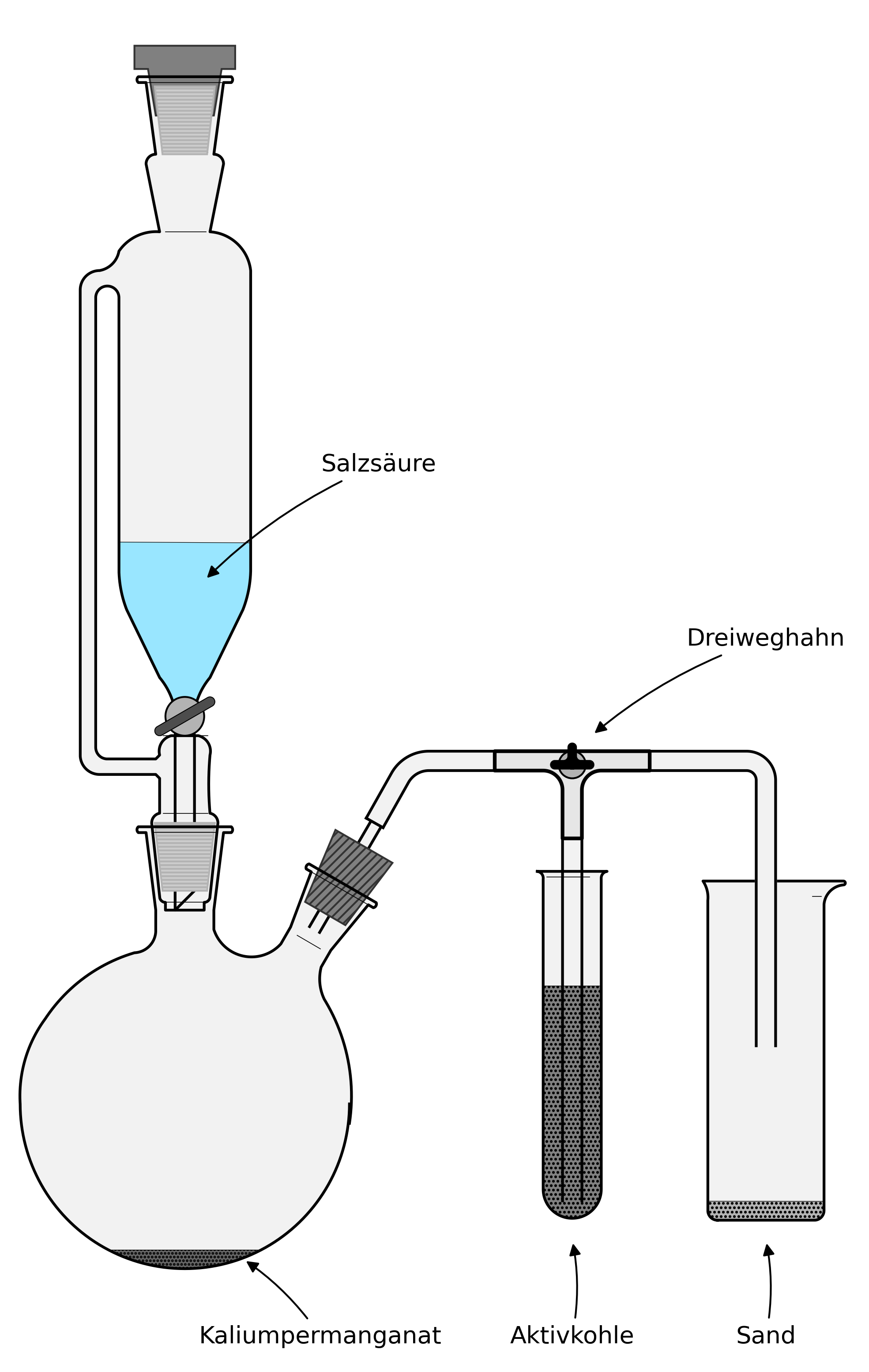
Herstellung von Chlorgas. Die Verzweigung zur Aktivkohle ist optional. Die Aktivkohle verhindert das Entweichen von Chlorgas, der Dreiweghahn darf aber nie ganz geschlossen werden. Zu Beginn ist der Dreiweghahn wie gezeigt so eingestellt, dass das Chlorgas in den Standzylinder fliesst
Zur Entwicklung des Chlorstroms lässt man langsam Salzsäure auf das kaliumpermanganat tropfen. Für die Versuche in diesem Abschnitt muss der Zylinder nur zu 3/4 mit Chlorgas gefüllt werden. Wenn die Chlorentwicklung gestoppt werden soll, wird die Salzsäurezufuhr gestoppt und das noch entweichende Chlor über den Dreiweghahn in die Aktivkohle geleitet. Stets nur mit Piktorgramm mit Gefahrensymbol (eines von beiden) in Schülerbereiche Stellen

H.2 Reaktion von Chlorgas mit organischen Stoffen¶
- Chlorgasgefüllter Zylinder (siehe oben) im ABZUG (Maturitätsarbeitszimmer) mit Warn-Piktogramm
- Filterpapier
- Terpentinöl
- Tiegelzange
- Latex-Handschuhe
!!Im ABZUG!! Am besten in einem Nebenzimmer, das man nach dem Versuch verlassen kann: In den mit Chlor gefüllten Zylinder taucht man mit der Tiegelzange einen mit Terpentinöl getränkten Filterpapierstreifen. Das Terpentinöl entzündet sich von selbst und brennt unter Russentwicklung.
Option: eine brennende Kerze in das Chlorgas senken. Die Kerze brennt weiter, beginnt aber zu nebeln und zu russen.
H.3 Reaktion von Chlorgas mit Eisenwolle (und Kupferwolle)¶
- Chlorgasgefüllter Zylinder (siehe oben) im ABZUG (Maturitätsarbeitszimmer) mit Warn-Piktogramm
- Stahlwolle = Stahlwatte
- Optional: Kupferwolle (dann aber mit zweitem chlorgasgefülltem Zylinder)
- Optional: Antimonpulver
- Gasbrenner mit Feuerzeug
- Tiegelzange
- Latex-Handschuhe
!!Im ABZUG!! Am besten in einem Nebenzimmer, das man nach dem Versuch verlassen kann: In den Zylinder brennende oder angewärmte Stahl- oder Kupferwolle geben. Sie brennt im Chlorgas gut.
Durchführung und Hinweise
H.2 Reaktion von Chlorgas mit organischen Stoffen¶
- Mit Terpentinöl getränkten Filterpapierstreifen in den chlorgefüllten Zylinder tauchen
- Terpentinöl entzündet sich und verbrennt unter Russentwicklung
- Chlor bildet in der Reaktion günstiges HCl, ist also in der Lage, gebundene Wasserstoffatome aus organischen Stoffen "herauszureissen". Die Kohlenstoffatome bleiben mehr oder weniger als elementarer Kohlenstoff zurück, daher die Russbildung. Bei knappem Cl₂ ist das am günstigsten:
- 1 CH₄ + 2 Cl₂ → 1 C (s) + 4 HCl
- ΔHᵣ = -294.42 kJ/mol, pro Cl₂ also -147 kJ/mol
- ΔSᵣ = 100.98 J/mol/K
- ΔGᵣ = -324.53 kJ/mol
- 1 CH₄ + 1 Cl₂ → 1 CH₃Cl + 1 HCl
- ΔHᵣ = -103.50 kJ/mol, pro Cl₂ also -103 kJ/mol
- ΔSᵣ = 2.58 J/mol/K
- ΔGᵣ = -104.27 kJ/mol
- 1 CH₄ + 2 Cl₂ → 1 CH₂Cl₂ + 2 HCl
- ΔHᵣ = -234.00 kJ/mol, pro Cl₂ also -117 kJ/mol
- ΔSᵣ = -100.78 J/mol/K
- ΔGᵣ = -203.96 kJ/mol
- 1 CH₄ + 4 Cl₂ → 1 CCl₄ + 4 HCl
- ΔHᵣ = -422.618 kJ/mol, pro Cl₂ also -106 kJ/mol
Möglicherweise kann man mit demselben Chlorgaszylinder den nächsten Versuch machen, wenn man das Filterpapier im Chlor nur anzündet, aber nicht verbrennen lässt.
H.3 Reaktion von Chlorgas mit Eisenwolle (und Kupferwolle)¶
- Standzylinder wird am Boden mit Sand bedeckt und mit Chlor gefüllt
- In den Standzylinder gibt man "angewärmte" oder an einem Ende entzündete Stahlwolle
- Der Versuch lässt sich auch mit Kupferwolle oder gepulvertes Antimon (ohne Erwärmung) durchführen
- Die Proben verbrennen unter Feuererscheinungen. Dabei entweicht Chlor: der Versuch muss natürlich im Abzug gemacht werden, wenn möglich in einem Nebenzimmer (MAA-Zimmer), das man anschliessend verlassen kann.
- 2 Fe + 3 Cl₂ → 2 FeCl₃
- ΔHᵣ = -799.0 kJ/mol
- ΔSᵣ = -469.198 J/mol/K
- ΔGᵣ = -659.10 kJ/mol
- 1 Cu + 1 Cl₂ → 1 CuCl₂
- ΔHᵣ = -220.1 kJ/mol
- ΔSᵣ = -158.116 J/mol/K
- ΔGᵣ = -172.96 kJ/mol
- 2 Sb + 3 Cl₂ → 2 SbCl₃ (s)
- ΔHᵣ = -766 kJ/mol
Material
Durchführung und Hinweise



Sicherheit¶
Sicherheitshinweise
Weiteres¶
Infos
- Nanoo-Zugang: nanoo.tv/sso/waad/
- Zugangslink, Video, Metadaten