Oxidationszahlen und organische Redox-Reaktionen¶
Material, Chemikalien und Hinweise¶
G Oxidationszahlen¶
Material
G.1 Pulsierendes Herz¶
- Kiste Pulsierendes Herz
- Abdampfschale,
- Feuerzeug
- Kartuschen-Gasbrenner
- Methanal-Lösung (Formalin)
G.2 Gummibärchen in der Feuerhölle¶
- Gummibärchen
- Grosses Duran-RG in alter RG-Klemme
- Musik, Becherglas als Tribüne, weisser Spot
- Pinzette
- Kaliumchlorat
- Kartuschen-Gasbrenner
G.3 Kupfer in Salpetersäure¶
- Natriumnitratlösung 0.1M mit Tropfpipette
- Salpetersäure
- Kupfer-Stück
- Euro-Cent
- 10 Rappen-Stück
- 3 kleine Bechergläser
G.4 Schwefel mit Kaliumchlorat (zu Thema Oxidationszahl)¶
- Kaliumchlorat
- Schwefel
- 2 Polylöffel
- ALTER Mörser und Pistill
- Schutzhandschuh (Gartenhandschuh)
- Ohrenschutz
- Schutzbrille
- Labormantel
- Schutzplatte
G.5 Roter Phosphor mit Kaliumchlorat¶
- Schutzplatte
- zusätzlichk kleine feuerfeste Schutzplatte aus Eternit (muss Schlag mit Hammer ertragen)
- Roter Phosphor mit Polylöffel auf Papierserviette
- Kaliumchlorat mit Polylöffel auf Papierserviette
- Hammer
G.6 Vergärung von Glucose¶
- Sirup
- Hefe
G.7 Vergärung von Glucose: Rootbeer mit Hefe¶
Pro Gruppe
- Bügelflasche (Bier) 0.1 L oder PET-Flasche. VORSICHT: Bügelflaschen sind so gasdicht, dass sie bei Überdruck explodieren. Gärung nur kurz laufen lassen, oder dann mit offenen Flaschen im Kühlschrank!
- Gärröhrchen in Loch-Stopfen (so, dass es auf die Flasche passt)
- ½ Trockenhefe mit Kaffeelöffel
- 2 Bierflaschen 0.5 L mit Bügelverschluss
- Lebensmittelechter Trichter
- 200g Haushaltszucker mit Messbecher ca 2 dl
- 1 Zitrone
- Saftpresse (es können sich auch zwei Gruppen eine Saftpresse teilen)
- Ingwer ca 20 g. Den Ingwer mit einem Schneidebrett und einem Küchenmesser pro Klasse bereitstellen.
- Feine Raffel (für Ingwer)
- Grosses Sieb
- Schneidebrett
- Küchenmesser
Durchführung und Hinweise
G.4 Schwefel mit Kaliumchlorat (zu Thema Oxidationszahl)¶
Durchführung: Linsengrosses bis erbsengrosses Häufchen Schwefel und etwa gleich viel Kaliumchlorat in die Reibschale geben, zuerst ganz fein, dann heftiger zerreiben (Lederhandschuhe!!). Schon wenn nur die Hälfte losgeht, gibt es einen gewaltigen Knall. Reibschale kann dabei in Brüche gehen.
3 S₈ + 16 KClO₃ → 24 SO₂ + 16 KCl auch ohne Redox gut lösbar S₈ + 16 KClO₃ → 8 SO₂ + 16 KClO₂
Lösbar, wenn man sich überlegt, wie viele O pro Chlorat-Ion abgespalten werden.
G.5 Roter Phosphor mit Kaliumchlorat¶
Ca. Linsen- bis Erbsengrosse Menge Kaliumchlorat auf Schutzplatte, darüber etwa gleich viel roter Phosphor, nicht vermischen! Mit Hammer draufschlagen (muss nicht fest sein, es knallt aber mehr beim festen Schlagen)
Produkte: P₂O₅ und KCl
G.6 Vergärung von Glucose: Rootbeer mit Hefe¶
Vorsicht: beim Arbeiten sollen möglichst wenig Keime in den Gäransatz gelangen, um Fehlgärungen zu vermeiden. Vorsicht: Nach ein paar Tagen baut sich in den Flaschen ein hoher Druck auf, der auch Bügelflaschen zum Bersten bringt.
- In eine gereinigte und trockene PET-Flasche ober Bügelflsche werden mit Hilfe eines Trichters 1.5 bis 2 dL (ein gefüllter Plastic-Becher) Haushaltszucker eingefüllt.
- Nun wird ¼ Teelöffel Hefe zugegeben, der Deckel verschlossen und die Flasche heftig geschüttelt.
- Einige Blätter Pfefferminze zugegeben.
- 1 Esslöffel geraffelter Ingwer und Saft einer gepressten Zitrone werden in die PET-Flasche gegeben.
- Die Flasche wird zu 7/8 mit Hahnenwasser gefüllt, verschlossen und erneut kräftig geschüttelt
- Die Flasche wird mit einem Gärröhrechen verschlossen, das Gärröhrchen mit heissem Wasser gefüllt und der Ansatz für rund 12-24 h an einem warmen Ort aufrecht gelagert. Druck regelmässig kontrollieren. Wenn der Gärprozess länger dauern soll: im Kühlschrank lagern! Es ist sehr gefährlich, diese Gärung in einer verschlossenen Flasche zu machen, auch dickwandige Glasflaschen oder PET-Flaschen können dabei gesprengt werden.
- Am Schluss für ein paar Stunden im Kühlschrank gären lassen. Wenn der Druck regelmässig kontrolliert wird, kann die Flasche verschlossen werden, nachdem die Gärung nachlässt.
- Die Flasche wird optisch geprüft, vorsichtig geöffnet und ein Geruchstest vorgenommen.
- Falls nötig, wird das Getränk gesiebt (Sieb und Trichter). Entstanden ist ein leicht alkoholhaltiges, moussierendes Getränk
- Prost!
Quellen:
Sandor Ellix Katz: Die Kunst des Fermentierens, Kopp Verlag 2017 http://www.chefhansen.de/2014/07/14/hausgebrautes-ginger-beer-mit-ginger-bug/ https://nourishedkitchen.com/ginger-bug/
H. Kaliumpermanganat Einführung¶
Material
H.1 Oxidierende Wirkung von KMnO₄ und pH¶
Pro Klasse
- KMnO₄-Lösung 0.02 mol/L (= 3.16 g/L; es reichen 20 ml)
- Gesättigte NaCl-Lösung in Tropfflasche
- Konzentrierte Salzsäure mit Tropfpipette im Abzug.
- Konzentrierte Schwefelsäure mit Tropfpipette im Abzug.
- Kartonschachtel mit RG
- Tropfflasche mit Natriumthiosulfat (0.1M).
Pro Gruppe
- RG-Ständer
H.2 Reaktivität des Permanganat-Ions: Blitzlicht mit Verzögerung¶
- 7.5 g Kaliumpermanganat
- 3.75 g Magnesiumgriess
- 2 Reibschalen mit Pistill
- 1-1.5 mL trockenes Glycerin mit Tropfpipette
- Feuerfeste Unterlage
- Spatel
- Erlenmeyerkolben 250 mL Weithals.
H.2 KMnO₄ und Cyclohexen¶
Pro Klasse
- KMnO4-Lösung 0.02 mol/L (= 3.16 g/L; es reichen 20 ml)
- Konzentrierte Schwefelsäure mit Tropfpipette im Abzug.
- Konzentrierte Natronlauge mit Tropfpipette im Abzug
- Kartonschachtel mit RG
- Tropfflasche mit Cyclohexen.
- KMnO4 (s) mit Spatel
- Dichlormethan mit Tropfpipette
- Kronenether 18-crown-6 mit Spatel
Pro Gruppe
- RG-Ständer
J Oxidation von Alkoholen durch KMnO₄¶
Material
Primäre, sekundäre und tertiäre Alkohole unterscheiden sich in ihrer Oxidierbarkeit. Bei diesem Projektionsversuch wird als Oxidationsmittel Kaliumpermanganat verwendet, das bei den unterschiedlichen Alkoholen verschiedene Oxidationsstufen erreicht und dies durch die jeweilige Färbung anzeigt.

Material:¶
- Petrischalen (ggf. eine dreifach geteilte),
- Messzylinder,
- BG 50 mL,
- Pasteurpipetten
- Propan-1-ol (n-Propanol)
- Propan-2-ol (Isopropylalkohol)
- Methylpropan-2-ol (tert-Butanol)
- Kaliumpermanganat-Lösung 0.006 M (0.10 g / 100 mL)
- Natronlauge, 1M.
Durchführung und Hinweise
Durchführung¶
- 15 ml KMnO4-Lösung mit 15 ml Natronlauge versetzen und die Lösung gleichmässig auf die drei Schalen bzw. die drei Felder einer gedrittelten Schale verteilen (Auf Hellraumprojektor). - In die Schalen nun je eine Pipettenfüllung eines der verschiedenen Alkohole geben und gut durchmischen.
- Bei 1- und 2-Propanol tritt sofort eine Grünfärbung auf, bei 1-Propanol schlägt die Farbe innerhalb einer Minute nach braun um. Bei tert. Butanol zeigt sich keine Farbänderung.
Erklärung:¶
Primäre Alkohole können durch Permanganat bis zur Carbonsäure oxidiert werden, sekundäre Alkohole bis zum Keton. Dabei werden, ausgehend vom violetten MnVIIO4-, die Oxidationsstufen +VI (grün) und ggf. +IV (braun) erreicht. Tertiäre Alkohole wirken auf Permanganat nicht reduzierend, die Lösung bleibt violett.
Nachtrag:¶
Die vorstehende Erklärung ist so in der Literatur beschrieben, nachvollziehbar und didaktisch sinnvoll. Es ist aber überraschend, daß die Menge der zugesetzten Alkohole offenbar kaum eine Rolle spielt. Nach einiger Zeit färbt sich auch die Lösung mit dem sekundären Alkohol bräunlich, auch wenn sie isoliert steht. Die Ursache für das unterschiedliche Verhalten ist eine andere: Zu Beginn liegt eine stark basische KMnO4-Lösung vor. In diesem Milieu ist nur eine Reduktion zum Manganat(VI) möglich. Bei der Oxidation des primären Alkohols entsteht eine Carbonsäure, wodurch die Natronlauge teilweise neutralisiert wird. Der pH-Wert fällt und es kann sich auch Braunstein bilden. Die pH-Änderung kann auch durch eindiffundierendes Luft-CO2 erfolgen, daher sollten die Schalen vor Versuchsdurchführung abgedeckt und der Versuch rechtzeitig abgebrochen werden.
Gefahren:¶
Die Alkohole sind leichtentzündlich und beim Einatmen gesundheitsschädlich. Kaliumpermanganat ist brandfördernd, Natronlauge ätzend.
Entsorgung: Die Lösungen kommen zum Schwermetall-Abfall.
Literatur & Links:¶
Roland Full, Werner Ruf: "Vom Reagenzglas in die Petrischale", Naturwissenschaften im Unterricht: Chemie, 10 (1999), Nr. 51, 37-39 Roland Full: "Lichtblicke - Petrischalenexperimente in der Overhead-Projektion" Chemie in unserer Zeit, 30 (1996), 286-294
K Mineralisches Chamäleon¶
Material

- Becherglas 1L, hohe form
- kleine Bechergläser
-
Messpipette.
-
0.33 g Kaliumpermanganat in 100 ml Wasser, Viel zu konzentriert. 0.033 g/100mL probieren
- 10 ml 50%ige Natronlauge + 10 ml 1%ige Natriumformiat-Lösung,
- halbkonzentrierte Schwefelsäure,
- 1%ige Natriumsulfit-Lösung.
Durchführung und Hinweise
| Redox-Reihe für pH=0 | E° (pH 0) | Redox-Reihe für pH=14 | E° (pH 14) | ||
|---|---|---|---|---|---|
| 0 | [V] | [V] | |||
| 1 | Mn(OH)₂ + 2 OH⁻ ⇄ MnO₂ + 2 H₂O + 2 e⁻ | -0.04 | |||
| 2 | Mn(OH)₂ + 6 OH⁻ ⇄ MnO₄⁻ + 4 H₂O + 5 e⁻ | 0.34 | |||
| 3 | Verschiedene mit ClO₂⁻ ClO₄⁻ | Um 0.3 | |||
| 4 | 2 I⁻ ⇄ I₂ + 2 e⁻ | 0.54 | 2 I⁻ ⇄ I₂ + 2 e⁻ | 0.54 | |
| 5 | MnO₄²⁻ ⇄ MnO₄⁻ + 1 e⁻ | + 0.56) | MnO₄²⁻ ⇄ MnO₄⁻ + 1 e⁻ | 0.56 | |
| 6 | HMnO₄⁻ ⇄ MnO₄⁻ + H⁺ + 1 e⁻ | 0.9 | |||
| 7 | |||||
| 8 | MnO₂ + 4 OH⁻ ⇄ MnO₄⁻ + 2 H₂O+ 3 e⁻ | 0.59 | |||
| 9 | MnO₂ + 4 OH⁻ ⇄ MnO₄²⁻+ 2 H₂O+ 2 e⁻ | 0.6 | |||
| 10 | Br⁻ + 6 OH⁻ ⇄ BrO₃⁻ + 3 H₂O+ 6 e⁻ | 0.61 | |||
| 11 | Cl⁻ + 6 OH⁻ ⇄ ClO₃⁻ + 3 H₂O+ 6 e⁻ | 0.62 | |||
| 12 | 2 Br⁻ ⇄ Br₂ + 2 e⁻ | 1.09 | 2 Br⁻ ⇄ Br₂ + 2 e⁻ | 1.09 | |
| 13 | Mn²⁺ + 2 H₂O ⇄ MnO₂ + 4 H⁺+ 2 e⁻ | 1.23 | |||
| 14 | 2 Cl⁻ ⇄ Cl₂ + 2 e⁻ | 1.36 | 2 Cl⁻ ⇄ Cl₂ + 2 e⁻ | 1.36 | |
| 15 | Mn²⁺ + 4 H₂O ⇄ MnO₄⁻ + 8 H⁺+ 5 e⁻ | 1.51 | |||
| 16 | MnO₂ + 2 H₂O ⇄ MnO₄⁻ + 4 H⁺+ 3 e⁻ | 1.69 | |||
| 17 | MnO₂ + 2 H₂O ⇄ HMnO₄⁻ + 3 H⁺+ 2 e⁻ | 2.09 | |||
| 18 | (MnO₂ + 2 H₂O ⇄ MnO₄²⁻ + 4 H⁺ + 2 e⁻ | + 2.25) |
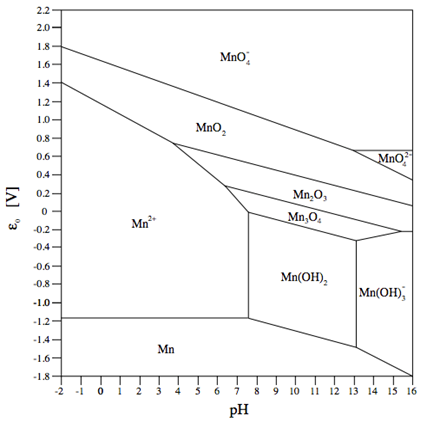
Die Farbänderungen bei der Redox-Chemie des Mangans sind bereits seit dem 17. Jhd. bekannt. Die Bezeichnung "Mineralisches Chamäleon" geht auf den Entdecker des Sauerstoffs, C. W. Scheele (1742-86), zurück. Johann Wolfgang Döbereiner führte das Mangan-Chamäleon seinem Freund Johann Wolfgang von Goethe vor, letzterer verarbeitete den Versuch in seiner Farbenlehre. Das Experiment basiert auf der schrittweisen Reduktion des violetten Permanganat-Ions (Oxidationsstufe +VII) über +VI (grün), +V (blau), +IV (braun) zum fast farblosen zweiwertigen Mn2+.
- 10 ml der Kaliumpermanganat-Lösung (1) in das Becherglas geben, mit Wasser auffüllen und umrühren. Im Folgenden wird nicht mehr gerührt.
- Lösung (2) eingießen, diese sinkt nach unten, wobei sich die violette KMnO4-Lösung von unten nach oben blau färbt, gefolgt von einer Grünfärbung. Hat nicht funktioniert, vermutlich zu wenig (1L Messzylinder). Mindestens doppelte Menge nehmen
- Nun 10 ml halbkonzentrierte Schwefelsäure (3) mit einer Pipette unterschichten. Die grüne Farbe schlägt im unteren Bereich nach braun um. Unterschichten geht mit normaler Pipettierhilfe nicht – stattdessen füllt sich die Pipette. Man müsste einen alten Peleusball nehmen, mit dem man auch blasen kann.
- Nach Unterschichten mit 5 ml Lösung (4) entfärbt sich die braune Lösung teilweise. Alle Vorgänge brechen ab, bevor die gesamte Lösung umschlägt, daher stehen am Ende fünf verschiedenfarbige Zonen übereinander. Gleiches Problem: Unterschichten geht nicht ohne Peleusball.
- Da sich die Lösungen kaum einbringen liessen, habe ich zwei mal ca ½ Polylöffel festes Natriumsulfit zugegeben. Nach dem Absinken waren grünblau, braun, farblos, intensiv rot gut zu sehen.
Erklärung¶
Das violette Permanganat-Ion (Mn(VII)O₄⁻) wird nach und nach reduziert.
Durch die alkalische Formiat-Lösung entsteht vermutlich zunächst blaues Hypomanganat (Mn(V)O₄³⁻), das jedoch nicht stabil ist und durch noch vorhandenes Permanganat zum grünen Manganat (Mn(VI)O₄²⁻) oxidiert wird. (Eine Disproportionierung des Hypomanganats ist unwahrscheinlich, da in diesem Fall Braunstein (Mn(IV)O₂) ausfallen würde.) Die schmale blaue Grenzschicht entsteht vermutlich als Mischfarbe von Manganaten in verschiedenen Oxidationsstufen. Beim Ansäuern erfolgt nun eine Disproportionierung des grünen Manganats(VI) zu violettem Permanganat und gelbbraunem Manganit (Mn(IV)O₄⁴⁻). Man beobachtet als Mischfarbe ein rotbraun. Durch starke Reduktionsmittel, z.B. Sulfit (SO₃²⁻), kann Manganit(IV) zum zweiwertigen Mangan-Kation (schwach rosa) reduziert werden.