Einführung Säure/Base-Chemie¶
Material, Chemikalien und Hinweise¶
A. Welches Teilchen bewirkt den sauren Geschmack?¶
Material
Folgende Lösungen - in Lebensmittelqualität (Ph. Eur.) jeweils 100 mL bereitstellen, - jeweils angemacht in einem lebensmittelechten Gefäss (z.B. Pappebecher) - mit je einem lebensmittelechten Löffeln in jedem dieser Gefässe zum Entnehmen. - Dazu pro Schüler ein Löffel zum Degustieren (SuS entnehmen Probe mit dem Löffel in der Chemikalie, überführen die Probe in den eigenen Löffel und stecken diesen dann in den Mund) - Reagenzglasständer mit 8 Reagenzgläsern - Universalindikatorlösung
Konzentrationen:
- Feststoffe:
- Kochsalz und Vitamin C: ziemlich konzentriert,
- alle anderen: eine Löffelspitze pro 100 mL.
- Mineralwasser: unverdünnt
-
Andere Lösungen:
- Verdünnt auf dreifaches Volumen
-
Wasser (Leitungswasser verwenden!! Nicht deionisiertes Wasser)
- Ammoniumkarbonat („Treibsalz“)
- HCl(aq), stark verdünnt höchstens 10mM bzw. 0.03% !!
- Mineralwasser (unverdünnt)
- Soda (Natriumcarbonat)
- Kochsalz
- Vitamin C
- Speiseessig
Zudem bitte räumlich getrennt (hat keine Lebensmittelqualität und darf nicht probiert werden)
- Natronlauge 0.1 M
Durchführung und Hinweise
Die SuS sollen sich überlegen,
- welche Lösungen sauer schmecken
- ob OH⁻ einen Geschmack haben.
- und sollen anhand der Auflistungen aller Teilchensorten aller Lösungen herausfinden, welche Teilchensorte den sauren Geschmack bewirkt.
B. Reaktivität von sauren und basischen wässrigen Lösungen: Auflösen von Aluminium¶
Material
- 3 BG hohe Form 50 mL
- 3 BG hohe Form 100 mL
- HCl (conz)
- NaOH (conc)
- Universalindikator
- Alufolie
- Puffer pH 7
- flache Wanne als Unterlage
- Grosses RG in RG-Ständer
Durchführung und Hinweise
Es geht hier um die Teilchen H₃O⁺ und OH⁻. H₃O⁺ ist das Teilchen, welches Lösungen sauer schmecken lässt. Es ist sehr reaktiv. Ein anderes Teilchen aus denselben Atomsorten ist ebenfalls sehr reaktiv, dies zeigt folgendes Experiment OH⁻
In einem BG 50 mL liegt schon etwas Salzsäure + Puffer ca. 5:1 vor. Ein Teil dieser Lösung wird in ein anderes BG gegeben und Universalindikator Alufolie zugegeben. Die Alufolie löst sich auf (solange die Reakion heftig ist, gut zudecken mit einem umgedrehten 100 mL BG). Im Abzug oder wo sehr gut lüftbar (Maturaarbeitszimmer). Auch die konzentrierte NaOH mit Universalindikator vermag das Alu aufzulösen, wenn auch langsamer (die Korundschicht lässt sich mit Lauge weniger schnell entfernen als mit Säure).
Man Schmeckt H₃O⁺, aber da Säuren sehr aggressiv sein können, brauchen wir einen alternativen Nachweis als unsere Zunge - Zusatz von Universalindikator und etablierung der Farben Rot - Grün - Blau.
Fazit: Saure Lösungen sind sehr reaktiv. Basische auch. Dann müsste doch ein Gemisch aus Beidem noch viel reaktiver sein?
Nun wird die verbleibende mit etwas Puffer versetzte HCl mit Universalindikator und so lange mit Natronlauge versetzt, bis die Farbe grün ist. Nun löst sich das Alu in der Lösung nicht mehr auf. Vorsicht: Gewisse Farbstoffe des Universalindikators werden zumindest in der konzentrierten Lauge schnell abgebaut, daher den Universalindikator eher der Säure zusetzen und diese mit Lauge neutralisieren.
Die Vormischung ist nur für den dritten Versuch erforderlich (Neutralisation). An sich reagiert die reine Salzsäure effektvoller mit dem Aluminium. Durch den Zusatz von etwas Puffer kann man aber beim Neutralisieren tatsächlich auch einen neutralen pH erreichen, sonst wäre das mit den konzentrierten Lösungen nicht möglich. Die Verwendung des Puffers hier nicht thematisieren.
Spaghetti kochen auf chemisch: In einem Grossen RG werden wenige mL NaOH (conz) vorgelegt und vorsichtig und langsam etwa gleich viel HCl (conz) zugegeben. SuS überprüfen Temperatur. Was ist die Fällung? Ist die Lösung noch gefährlich? Es ist direkt heisses Spaghettiwasser entstanden!
C. Reaktivität von sauren und basischen wässrigen Lösungen: Reaktion mit Zink zu Wasserstoff¶
Material

- Zinkpulver mit Spatel auf Papierserviette
- Salzsäure 1:4
- Grosses Reagenzglas in passendem Reagenzglasständer
- Passender Stopfen mit Loch und eingepasstem Glasrohr
- kleines RG
- Feuerzeug
Durchführung und Hinweise
Dieses Experiment ist eigentlich ein Redox-Experiment. In diesem Kontext zeit es einfach, dass Säuren auch Metalle angreiffen, was man bereits mit Experiment A sieht. Also kann es gut weggelassen werden
Ein guter Spatel Zinkpuver wird in eine wässrige Lösung mit leicht verdünnter Salzsäure (1:4) (\(H_2O^+\) und \(Cl^-\)) gegeben. Das Gemisch schäumt auf, das Metall wird „zerfressen“. Das Gas kann mit einem zweiten RG aufgefangen und untersucht werden. Zu diesem Zweck hält man ein offenes Reagenzglas, welches das gesammelte Gas enthält, in die Bunsenbrennerflamme. Unter Umständen brennt das Gas ruhig ab, u.U. verbrennt es mit einem kurzen Puff oder Pfiff.
☠
Keinesfalls darf der Wasserstoff im Gummistopfen und Glasrohr verschlossenen Reagenzglas angezündet werden. Das Reagenzglas könnte explodieren
Um welches Gas könnte es sich handeln? Tipp: Metall-Atome geben bereitwillig Elektronen ab (und werden dabei zu Kationen).
D. Synthese und Untersuchung von HCl (g)¶
Material
Ein mal im Abzug bereitstellen
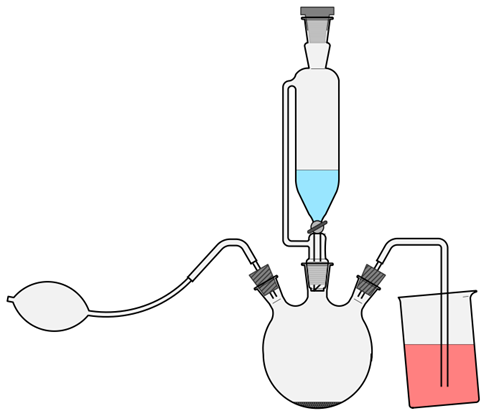
Synthese¶
- 1 Tropftrichter 50 mL mit Druckausgleich
- 3-Hals-Rundkolben
- Einleitungsrohr (Übergangsstück, Schlauch mit Paseurpipette)
- DC-Pümpeli
- Natriumchlorid mit Polylöffel
- Schwefelsäure (conc.)
- Apparatur gemäss Abbildung mit Schliffklemmen gesichert. Wenn möglich ohne Hahnen (ausser beim Tropftrichter 😊)

Untersuchung¶
- 2 BG 100 mL hohe Form (bitte überprüfen: sie sollen gerade breit genug sein, damit die Elektroden des Leitfähigkeitsprüfers eintauchen können)
- Deionisiertes Wasser in Spritzflasche
- Heptan
- Universalindikator
- Leitfähigkeitsprüfer VSN (Lampe 220 V)
- Leitfähigkeitsprüfer Klingel mit angeschlossenen Kohleelektroden
Durchführung und Hinweise
Durchführung:
Synthese¶
- 3 Polylöffel NaCl werden in den Rundkolben gegeben.
- Schwefelsäure conz wird in den Tropftrichter gegeben.
- Schwefelsäure wird auf das NaCl getropft. Die Probe schäumt auf.
Untersuchung¶
- Wird reines Wasser den Strom leiten? Nein: es enthält keine mobilen Ladungsträger. Überprüfen.
- Wird reines Heptan den elektrischen Strom leiten? Nein, aus demselben Grund
- HCl ist leider ein Gas. Damit wir es untersuchen können, leiten wir es in Flüssigkeiten ein.
- HCl in Heptan leitet den elektrischen Strom nicht.
- Gemisch aus HCl und Wasser leitet den elektrischen Strom hingegen.
- Hier müssen also Ionen entstanden sein. Wie können welche Ionen entstanden sein? Ohne dass die Edelgasregel verletzt wird? Ein H-Kern springt von einem Molekül auf ein anderes. Welche Möglichkeiten gibt es? (HCl + H₂O → Cl⁻ + H₃O⁺ bzw. HCl + H₂O → H₂Cl⁺ + OH⁻).
- Überprüfung mit Universalindikator!
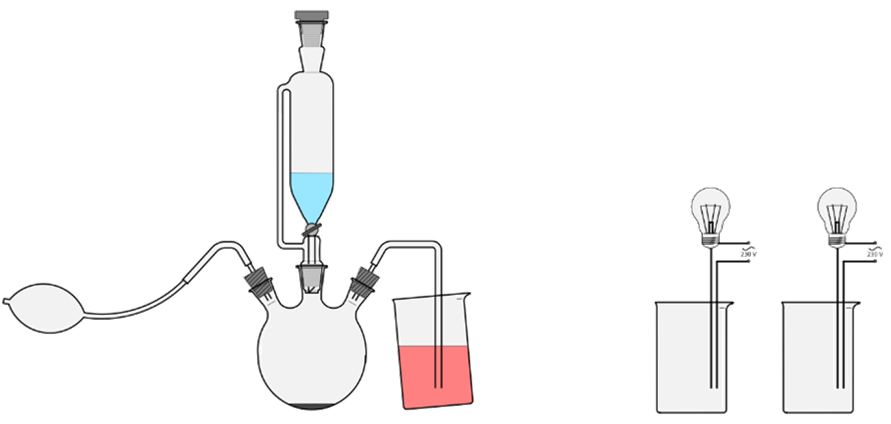
E. Ammoniak-Springbrunnen¶
Die ausführliche Variante sieht vor, dass man den Ammoniak in einem separaten Rundkolben erhitzt und verdampft, dann über einen Schlauch in den eigentlichen Rundkolben überführt und dann damit den Versuch macht. Das ist experimentell sehr aufwändig und funktioniert oftmals nicht sehr gut.
E.1 einfache Variante¶
Material
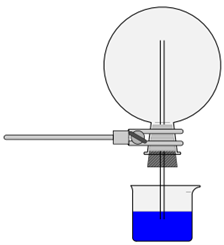
- Kristallisierschale Durchmesser ca. 20 cm.
- Rundkolben 500 mL mit passendem Stopfen mit Loch und eingepasstem kurzem Glasrohr (z.b. Glaspipette)
- Stativklammer und Handschuhe, um den Rundkolben zu halten
- Bunsenbrenner mit Feuerzeug
- Ammoniak conc. mit Tropfpipette in kleinem Erlenmeyer
- Universalindikator
Durchführung und Hinweise
- Die Kristallisierschale mit genug Wasser füllen, dass damit der ganze Rundkolben gefüllt werden kann. Das Wasser mit etwas Leitungswasser bei neutralem pH puffern und mit Universalindikator einfärben
- Einen Rundkolben mit etwas konzentriertem Ammoniak (5 mL) bestücken,
- Den Rundkolben mit einem Stopfen mit Loch und eingepasstem kurzem Glasrohr verschliessen
- Den Rundkolben über dem Bunsenbrenner kurz erhitzen, bis ein Teil der Flüssigkeit verdampft ist. Darauf achten, dass der Rundkolben dort, wor er erhitzt wird, niemals trocknet (sonst wird er zu heiss und das einströmende Wasser explodiert)
- Das Glasrohr in Wasser eintauchen - tief genug, dass sicher keine Luft eingesogen wird, wenn das Wasser im Rundkolben ist. Natürlich spielt dann der heisse Wasserdampf eine grössere Rolle als der gasförmige Ammoniak, der sich im Wasser löst.
E.2 komplizierte Variante¶
Material
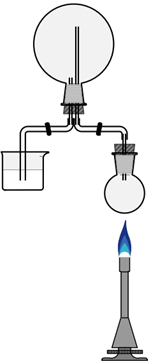
- Ein 1L-Rundkolben wird mit einem doppelt durchbohrten Stopfen mit zwei kurzen Glasrohren bestückt. An jedes Glasrohr wird ein Gummischlauch angeschlossen. Die Apparatur soll so zusammengestellt werden, dass diese Gummischläuche möglichst kurz sind.
- Phenolphthaleinlösung in becherglas (in deionisiertem Wasser, gepuffert mit wenig Leitungswasser),
- kleiner Rundkolben mit 5 mL Ammoniak conz., passender Stopfen mit Loch und kurzem Glasroht
- Die Apparatur wird mit einer Befestigungsvorrichtung für die Gummischläuche so zusammengestellt (in der Abbildung), dass der eine Gummischlauch in die Phenolphthaleinlösung eingetaucht werden kann, während der kleine Rundkolben mit dem anderen Gummischlauch angeschlossen werden kann,
- 2 Quetschhalme
- Bunsenbrenner
- Gumminuggi
Durchführung und Hinweise
- Ein 1L-Rundkolben wird mit einem doppelt durchbohrten Stopfen mit zwei kurzen Glasrohren bestückt.
- Das eine Glasrohr geht über Gummischlauch in eine Phenolphthaleinlösung (in deionisiertem Wasser, mit Leitungswasser auf neutralen pH gepuffert), das andere zu dem kleinen Rundkolben mit 5 mL Ammoniak conz.
- Die zwei schwarzen Striche auf den Schläuchen sind Quetschhalme, die noch nicht montiert werden.
-
Nun wird der konz. Ammoniak so lange erhitzt, bis sich die Phenolphthalein-Lösung verfärbt. Nun werden die Gummischläuche mit den Quetschhalmen verschlossen und alllenfalls unterhalb der Halme abgeschnitten. oder vom Glasrohr beim kleinen Rundkolben abgezogen
-
Für den Springbrunnenversuch wird der längere Schlauch in Wasser mit Phenolphthalein getaucht. An den kürzeren Schlauch kann ein Gumminuggi mit etwas Wasser angeschlossen werden. Einspritzen von Wasser ergibt einen unterdruck, was den Vorgang beschleunigt.
F. Bildung von Ammoniumchlorid¶
Material
Ist nun im Salz-Kapitel untergebracht
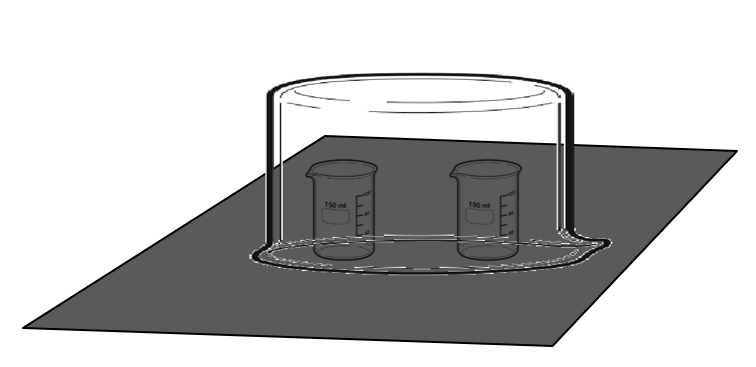
- Zwei kleine BG
- konzentrierter Ammoniak
- konzentrierte HCl
- möglichst grosse Kristallisierschale.
- Darunter in schwarzen Buchstaben NH₄Cl.
- Unterlage aus demselben Material wie die schwarzen Buchstaben
- Pinzette zum Entfernen der Buchstabe
Bei der Reaktion färbt sich der Boden weiss und man kann "das Experiment" dann fragen, welcher Stoff entstanden ist.
Durchführung und Hinweise
Zwei BG mit konzentriertem Ammoniak bzw. HCl unter Kristallisierschale. Darunter in schwarzen Buchstaben \(NH_4Cl\).
Bei der Reaktion färbt sich der Boden weiss und man kann das Experiment dann fragen, welcher Stoff entstanden ist.
G. Erst das Wasser, dann die Säure, sonst geschieht das Ungeheure¶
Material
☠ Stark ätzend, wird heiss und kann spritzen ☠
- Labormantel, Laborbrille, Latex-Handschuhe, geschlossene Schuhe, im Abzug arbeiten!
- Reagenzglas
- RG-Klammer
- Konzentrierte Schwefelsäure mit Tropfpipette in kleinem Erlenemeyer
- Vernier-Temperaturfühler (der in ein RG gehängt werden kann) mit allem, was es braucht, um den Temperaturfühler an den Comupter anzuschliessen.
Durchführung und Hinweise


☠ Stark ätzend, wird heiss und kann spritzen ☠
- Ziehe Latex-Handschuhe an
- Fülle ein Reagenzglas etwa 1 cm hoch mit Wasser
- Halte das RG mit einer RG-Klammer
- Gib nun Tropfen um Tropfen konzentrierte Schwefelsäure zu
- Beobachte und überprüfe die Temperatur mit dem Handrücken
- Optional: Temperatur mit Vernier-Messsonde verfolgen