Nachweisreaktionen¶
Material, Chemikalien und Hinweise¶
A. Organische Nachweisreaktionen Einführung¶
Material
Für die ganze Klasse
- Pro Gruppe ein RG-Ständer
- Wasserbad 50°C
- Schachtel mit vielen RG
Proben bitte doppelt, jeweils mit Tropfpipetten:
- Ethanol
- Essigsäure 1 M
- Essigsäureethylester
- Propan-1-ol
- Propansäure
- Heptan
- Propansäurepropylester. Falls nicht vorhanden bitte für die Zukunft bestellen und vorläufig Propionsäureethylester aufstellen. Da dieser verunreinigt ist, bitte vorgängig einmal mit Na₂CO₃ ca. 5% ausschütteln.
- Alltagsprodukt 1: Brennsprit (oder Melissengeist)
- Alltagsprodukt 2: Reinigungsmittel wie Fleckenteufel
Nachweisreagenzien¶
Posten 1: Cernitrattest:
- 40 g Cer(IV)-ammoniumnitrat in 100 mL Salpetersäure 2 M (pro Halbklasse 50 mL).
- Socorex 1 mL
- Socorex 2 mL
- Becherglas 500 mL
Posten 2: Bayer-Probe 1:
- Lösung I (0.1 g Kaliumpermanganat in 100 mL Wasser)
- Lösung III (Schwefelsäure 0.1 M).
- 2 Messzylinder 25 mL
- 1 Becherglas 100 mL
- Socorex 1 mL
Posten 3: BTB-Reagenz:
- 0.02 g Bromthymolblau und 0.6 g NaOH in 100 mL Ethanol
- Tropfpipette
Posten 4: Rojahn-Test:
- Ethanol mit Socorex 1 mL
- 1 Tropfflasche Phenolphthaleinlösung (0.1 g Phenolphthalein in 100 mL Ethanol)
- 100 mL NaOH 3 M mit Tropfpipette
Posten 5: Eisenchlorid-Test:
- 1 Tropfflasche Phenolphthaleinlösung (0.1 g Phenolphthalein in 100 mL Ethanol)
- Salzsäure (0.5 M) mit Tropfpipette
- NaOH (3 M) mit Tropfpipettte
- Eisenchloridlösung (8 g FeCl₃ · 6 H₂O in 100 mL Wasser) mit Tropfpipette
- Pentan-1-ol (Amylalkohol) mit Tropfpipette
NUR WENN AUSDRÜCKLICH GEWÜNSCHT: Posten 6: Iodoform-Probe:
- Iodreagenz (12.7 g Iod und 25.4 g Kaliumiodid mit Wasser auf 100 mL auffüllen) mit Tropfpipette
- 100 mL NaOH 3M mit Tropfpipette
B. Organische Nachweisreaktionen Miniquiz¶
Material
Für die ganze Klasse 1. Pro Gruppe ein RG-Ständer 2. Wasserbad 50°C 3. Schachtel mit vielen RG
Proben jeweils mit Tropfpipetten:
- Ethanol
- Essigsäure 1 M
- Essigsäureethylester
- Propan-1-ol
- Propan-2-ol
- Propansäure
- Heptan
- Propanon (Aceton)
- Alltagsprodukt 1: Brennsprit oder Melissengeist (bei mir zu haben)
- Alltagsprodukt 2: Reinigungsmittel wie Fleckenteufel (bei mir zu haben)
Unbekannte Proben mit Tropfpipetten, z.B. Beschriftet mit Buchstaben (in folgender Tabelle ein Vorschlag. Bitte bei Abweichung eine Lösung bereitlegen).
- Ethanol
- Ethansäure 1 M
- Ethansäureethylester
- Propan-1-ol
- Propansäure verdünnt
- Propansäurepropylester oder ähnlich
- Propan-2-ol
- Xylol : Cyclohexen = 3:1
Nachweisreagenzien¶
Posten 1: Cernitrattest:
- 40 g Cer(IV)-ammoniumnitrat in 100 mL Salpetersäure 2 M (pro Halbklasse 50 mL).
- Socorex 1 mL
- Socorex 2 mL
- Becherglas 500 mL
Posten 2: Bayer-Probe 1:
- Lösung I (0.1 g Kaliumpermanganat in 100 mL Wasser)
- Lösung III (Schwefelsäure 0.1 M).
- 2 Messzylinder 25 mL
- 1 Becherglas 100 mL
- Socorex 1 mL
Posten 3: BTB-Reagenz:
- 0.02 g Bromthymolblau und 0.6 g NaOH in 100 mL Ethanol
- Tropfpipette
Posten 4: Rojahn-Test:
- Ethanol mit Socorex 1 mL
- 1 Tropfflasche Phenolphthaleinlösung (0.1 g Phenolphthalein in 100 mL Ethanol)
- 100 mL NaOH 3 M mit Tropfpipette
Posten 5: Eisenchlorid-Test:
- 1 Tropfflasche Phenolphthaleinlösung (0.1 g Phenolphthalein in 100 mL Ethanol)
- Salzsäure (0.5 M) mit Tropfpipette
- NaOH (3 M) mit Tropfpipettte
- Eisenchloridlösung (8 g FeCl₃ · 6 H₂O in 100 mL Wasser) mit Tropfpipette
- Pentan-1-ol (Amylalkohol) mit Tropfpipette
Posten 6: Iodoform-Probe:
- Iodreagenz (12.7 g Iod und 25.4 g Kaliumiodid mit Wasser auf 100 mL auffüllen) mit Tropfpipette
- 100 mL NaOH 3M mit Tropfpipette
C. Untersuchung der Produkte der Bayer-Reaktion¶
Material
Oxidation
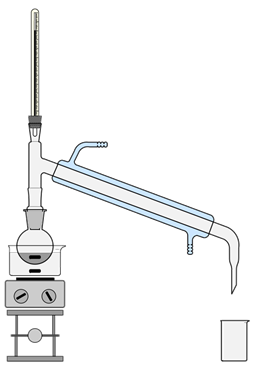
- Pro Klasse vier mal Material für ein eine Destillationsapparatur mit Ölbad (mit Schläuchen für Kühlung), aber nicht zusammengestellt.
- Oxidationsreagenz: pro Gruppe 50 mL KMnO4 5%, in 20% H₂SO₄
Proben, jeweils mit Tropfpipetten:
- Ethanol
- Essigsäureethylester
- Propansäurepropylester
- Propansäureethylester
- Propan-1-ol
- Propansäure (Überlegen lassen: macht Ansatz mit diesem Stoff Sinn?)
- Essigsäure (Überlegen lassen: macht Ansatz mit diesem Stoff Sinn?)
Für den Notfall, als ideale Reaktionsprodukte:
- Aceton
- Propan-2-ol
- Ca 20 mL Gemisch Ethanol + Essigsäureethylester 1+1, beschriftet mit "Probe A"
- Ca 20 mL Gemisch Ethanol + Essigsäure 1+1 beschriftet mit "Probe B"
- Ca 20 mL Heptan, beschriftet mit "Probe C"
- Ca 20 mL Gemisch Essigsäureethylester + Essigsäure 1+1.
Nachweisreagenzien¶
Posten 1: Cernitrattest:
- 40 g Cer(IV)-ammoniumnitrat in 100 mL Salpetersäure 2 M (pro Halbklasse 50 mL).
- Socorex 1 mL
- Socorex 2 mL
- Becherglas 500 mL
Posten 2: Bayer-Probe 1:
- Lösung I (0.1 g Kaliumpermanganat in 100 mL Wasser)
- Lösung III (Schwefelsäure 0.1 M).
- 2 Messzylinder 25 mL
- 1 Becherglas 100 mL
- Socorex 1 mL
Posten 3: BTB-Reagenz:
- 0.02 g Bromthymolblau und 0.6 g NaOH in 100 mL Ethanol
- Tropfpipette
Posten 4: Rojahn-Test:
- Ethanol mit Socorex 1 mL
- 1 Tropfflasche Phenolphthaleinlösung (0.1 g Phenolphthalein in 100 mL Ethanol)
- 100 mL NaOH 3 M mit Tropfpipette
Posten 5: Eisenchlorid-Test:
- 1 Tropfflasche Phenolphthaleinlösung (0.1 g Phenolphthalein in 100 mL Ethanol)
- Salzsäure (0.5 M) mit Tropfpipette
- NaOH (3 M) mit Tropfpipettte
- Eisenchloridlösung (8 g FeCl₃ · 6 H₂O in 100 mL Wasser) mit Tropfpipette
- Pentan-1-ol (Amylalkohol) mit Tropfpipette
Posten 6: Iodoform-Probe:
- Iodreagenz (12.7 g Iod und 25.4 g Kaliumiodid mit Wasser auf 100 mL auffüllen) mit Tropfpipette
- 100 mL NaOH 3M mit Tropfpipette
D. Umsetzung mit Natronlauge¶
Material
Pro Gruppe
- Eine Destillationsapparatur mit Ölbad (mit Schläuchen für Kühlung), aber nicht zusammengestellt.
- 4 Messzylinder 25ml
- Schott-Duran-Flasche 150 - 250 mL
- Socorex 10 mL
Pro Klasse
- ≥ 50 mL Essigsäureethylester
- ≥ 50 mL Essigsäurepentylester
- 15 mL Propansäureethylester (bereits 24h mit 60 mL NaOH 3M auf Magnetrührer)
- 15 mL Propansäurepropylester (bereits 24h mit 60 mL NaOH 3M auf Magnetrührer)
- Ethanol (zum Überlegen: macht es überhaupt Sinn, diese Probe zu testen.)
- Essigsäure
- Propansäure
- Propanol
- ≥ 500 mL NaOH 3 M mit Messzylinder 100 mL
- ≥ 50 mL Schwefelsäure 2 M mit Socorex 10 mL
Nachweisreagenzien¶
Posten 1: Cernitrattest:
- 40 g Cer(IV)-ammoniumnitrat in 100 mL Salpetersäure 2 M (pro Halbklasse 50 mL).
- Socorex 1 mL
- Socorex 2 mL
- Becherglas 500 mL
Posten 2: Bayer-Probe 1:
- Lösung I (0.1 g Kaliumpermanganat in 100 mL Wasser)
- Lösung III (Schwefelsäure 0.1 M).
- 2 Messzylinder 25 mL
- 1 Becherglas 100 mL
- Socorex 1 mL
Posten 3: BTB-Reagenz:
- 0.02 g Bromthymolblau und 0.6 g NaOH in 100 mL Ethanol
- Tropfpipette
Posten 4: Rojahn-Test:
- Ethanol mit Socorex 1 mL
- 1 Tropfflasche Phenolphthaleinlösung (0.1 g Phenolphthalein in 100 mL Ethanol)
- 100 mL NaOH 3 M mit Tropfpipette
Posten 5: Eisenchlorid-Test:
- 1 Tropfflasche Phenolphthaleinlösung (0.1 g Phenolphthalein in 100 mL Ethanol)
- Salzsäure (0.5 M) mit Tropfpipette
- NaOH (3 M) mit Tropfpipettte
- Eisenchloridlösung (8 g FeCl₃ · 6 H₂O in 100 mL Wasser) mit Tropfpipette
- Pentan-1-ol (Amylalkohol) mit Tropfpipette
Posten 6: Iodoform-Probe:
- Iodreagenz (12.7 g Iod und 25.4 g Kaliumiodid mit Wasser auf 100 mL auffüllen) mit Tropfpipette
- 100 mL NaOH 3M mit Tropfpipette
E. Demo und Auswertung Hydrolyse¶
Material
Demo-Experiment
- 2 Weithals-Erlenmeyer 100 mL
- Scheidetrichter 100 mL an Stativ
- 2 Bechergläser 200 mL
- 1 Messzylinder 100 mL
- Natriumsulfat wasserfrei mit Polylöffel
- Ethanol mit 20 mL Pipette oder Socorex 10 mL
- Propanol mit 20 mL Pipette oder Socorex 10 mL
- Ethansäure mit 20 mL Pipette oder Socorex 20 mL
- Propansäure mit 20 mL Pipette oder Socorex 20 mL
- Natriumhydrogencarbonatlösung 5%
Pro Gruppe:
- RG-Ständer
Durchführung und Hinweise Demo und Auswertung
- In einen 100 mL Weithalserlenmeyer
- 20 mL Alkohol geben (Ethanol oder Propan-1-ol)
- 20 mL Carbonsäure geben (Ethansäure oder Propansäure)
- 5 mL konzentrierte Schwefelsäure zugeben und gut schütteln
- 5 Minuten lang bei Raumtemperatur stehen lassen
- In 100 mL Scheidetrichter giessen, der bereits 110 mL Wasser enthält.
- Obere Phase wird mit ihrem doppelten Volumen an Natriumcarbonatlösung (1 M) versetzt und gut geschüttelt. Während des Schüttelns mehrfach vorsichtig zum Druckausgleich öffnen.
- Obere Phase nochmals mit ihrem eigenen Volumen an Wasser ausschütteln.
- Obere Phase wird in ein Becherglas überführt und mit wenig wasserfreiem Natriumsulfat getrocknet.
Ergebnisse:
- die Reaktionsansätze erwärmen sich stark
- Es entstehen rund 11.5 bis 12.5 mL Essigsäureethylester bzw. 19-20.5 mL Popionsäurepropylester
- Rojahn (stark schütteln) und Dichromattest /Bayer bei beiden positive
- Iodoform nur bei Essigsäureethylester positive, und nur leicht. Nach Zugabe von so viel Natronlauge, bis bei kräftigem Schütteln keine Braunfärbung mehr erkennbar ist, wird nochmals kräftig geschüttelt und das RG dann stehen gelassen. Bei kontinuierlicher BEobachtung kann man die Trübung gut sehen, es muss aber genau beobachtet warden.
F. Reagenzglasversuche Estersynthese¶
Material
Pro Klasse:
- Wasserbad auf ca. 90°C vorheizen.
- 5%-ige Natriumhydrogencarbonat-Lösung (mindestens 200ml) in Flüssigkeitsflasche mit aufgesetzter Dosierpumpe für 2ml-Portionen.
- 1 Schachtel Reagenzgläser
- Stopfen passend zu den Reagenzgläsern
In einem Abzug (sagen wir: Abzug A)
- Schwefelsäure konz.
Abzug B: je eine Flasche
- Salicylsäure rein mit Polylöffel auf Papierserviette
- Methanol mit Messpipette 5 mL und Pipettierhilfe
Abzug C: je eine Flasche
- Ethansäure (Essigsäure) mit Tropfpipette
- Propansäure (Propionsäure) mit Tropfpipette
- Zimtsäure mit Rinnenspatel
- Maleinsäure mit Rinnenspatel
Abzug D: je eine Flasche
- Konzentrierte Schwefelsäure mit Tropfpipette
- Pentan-1-ol (n-Pentanol) mit Tropfpipette
- 2-Methyl-propan-1-ol (Isobutylalkohol) mit Tropfpipette
- 3-Methyl-butan-1-ol (Isopentylalkohol, Isoamylalkohol) mit Tropfpipette
- Ethanol mit Tropfpipette
Nur wenn ausdrücklich bestellt: In Abzug B eine Flasche
- Pentansäure (Valeriansäure) mit Plastic-Tropfpipette auf Papiertuch
- Dazu ein Becherglas mit Natriumhydrogencarbonatlösung zum Auswaschen der Pipette.
(Originalflasche wegen Geruch in Konfitürenglas aufbewahren und mit Wegwerf-Handschuhen handhaben)
Durchführung und Hinweise Demo und Auswertung
- Versich mit Methansäure (Ameisensäure) nur als DEMO: Stark Ätzend
Methylsalicylat: Man soll 1 g Salicylsäure (M = 138.12 g/mol) verwenden und das Methanol ( = 0.79 g/mL) etwa im 3.5-fachen Überschuss einsetzen. Werte entweder angeben, oder: Wikipedia erlaubt. Rechnerisch: 5.14 mL Methanol.
Dann: wie mit der hohen Aktivierungsenergie umgehen? -Katalysator, Hohe Temperatur.
- Banane: Isopentylacetat ist charakteristisch, daneben haben auch Ester von Pentanol mit Essigsäure, Propionsäure und Buttersäure typisches Bananenaroma (aber kommen sie auch in der Banane vor?). (Ester des Hexanols und Butanols mit Essigsäure und Buttersäure werden als Fruchtig empfunden, aber auch in Banane?)
- Weintraube: die fruchtigen Noten: blumig-fruchtige Note bei amerikanischen Sorten: 2-Aminobenzoesäuremethylester
Orangen: (S)-2-Methylbuttersäureethylester, Buttersäureethylester, Isobuttersäureethylester, - Apfel: fruchtige Noten sind Essigsäureester (grün apfelartige Note: Aldehyde)
- Williamsbirne: Ethylester der (E,Z)-2,4-Decadiensäure, der (E)-2-Octensäure und der (Z)-4-Decensäure (aus Abbau ungesättigter Fettsäuren) sowie Essigsäurehexylester.
- Passionsfrucht: nebst Ionon: Ethylbutyrat, Ethylhexanoat, Hexylbutyrat, Hexylhexanoat
- Ananas: (S)-2-Methylbuttersäureethylester
- Erdbeeren: ein Furanon, dazu Ethyl- und Methyl-Ester von Buttersäure, Isobuttersäure und Methylbuttersäure.
- Pfirsich, Aprikose, Kirsche, Pflaume: Ester spielen keine grosse Rolle (aber teils Lactone = „Ringester“).
G. Hydrolyse und Kondensation¶
Material
Protease¶
- Voll belichteter, entwickelter Diafilm (bringe ich selber)
- Enzyrim Osa mit Subtilisin (starke Protease, wird zur Präparation von Skeletten verwendet). Andwendung: 10% Enzyrim Osa, 10% Tris-Puffer Ca. 8.5, 1 Schnipsel Diafilm
- 10% NaOH
- Es geht auch mit Pepsin: 10% Pepsin, 10% NaCl, 10% Tris-Puffer pH 8.5
Kohlenhydrate, Papiermaché¶
- Stärke (einfach etwas Mehl) und Malz zum Probieren.
Nylon-Seiltrick¶
In einem Abzug:
- In 50 mL Heptan gelöst: 2ml Sebacinsäuredichlorid (Decandisäuredichlorid) oder Adipinsäuredichlorid (Hexandisäuredichlorid)
- Wässrige Lösung von 2.17 g 1,6-Hexandiamin (Hexamethylendiamin) und 0.8 g NaOH in 50 mL Wasser (0.4 mol/L NaOH).
- 3 Bechergläser 200 mL
- Pinzette
- Universalindikator
- Latex-Handschuhe
- Phenolphthalein
- ggf. Gerät zum Aufwickeln des Fadens
Pro Gruppe
- Glasstab
Entsorgung: Keinesfalls in den Abguss!!!!! Kräftig umrühren, bis die Komponenten miteinander reagiert haben, dann im Abfall entsorgen. Früher: statt Heptan Chloroform. Versuch ging dann allerdings schief: vielleicht, weil Chloroform feucht, so dass Säurechlorid teilweise zerstört.